Γιατί τα ευγενή αέρια όχι από την ένωση εύκολα;
Εδώ είναι γιατί:
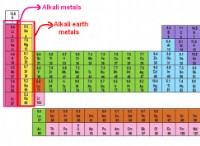
* Πλήρες εξωτερικό κέλυφος: Τα ευγενή αέρια έχουν ένα πλήρως γεμάτο εξωτερικό κέλυφος ηλεκτρονίων. Αυτή η διαμόρφωση είναι εξαιρετικά σταθερή, καθιστώντας τους απρόθυμους να κερδίσουν ή να χάσουν ηλεκτρόνια.
* Υψηλή ενέργεια ιονισμού: Η αφαίρεση ενός ηλεκτρονίου από ένα ευγενές άτομο αερίου απαιτεί σημαντική ποσότητα ενέργειας λόγω της σταθερής διαμόρφωσης ηλεκτρονίων. Αυτή η υψηλή ενέργεια ιονισμού καθιστά δύσκολο για αυτούς να σχηματίσουν θετικά ιόντα.
* χαμηλή συγγένεια ηλεκτρονίων: Τα ευγενή αέρια έχουν χαμηλή συγγένεια ηλεκτρονίων, που σημαίνει ότι δεν δέχονται εύκολα πρόσθετα ηλεκτρόνια. Αυτό οφείλεται στο γεγονός ότι το εξωτερικό τους κέλυφος είναι ήδη γεμάτο και η προσθήκη περισσότερων ηλεκτρόνων θα διαταράξει τη σταθερότητα.
Εξαιρέσεις:
Ενώ τα ευγενή αέρια είναι γενικά μη αντιδραστικά, υπάρχουν μερικές εξαιρέσεις:
* ενώσεις Xenon: Το Xenon, το μεγαλύτερο και πιο αντιδραστικό των ευγενών αερίων, σχηματίζει ενώσεις με εξαιρετικά ηλεκτροαρνητικά στοιχεία όπως το φθόριο και το οξυγόνο. Για παράδειγμα, XEF2, XEF4 και XEO3.
* ενώσεις ραδονίου: Το ραδονικό είναι ακόμα πιο αντιδραστικό από το Xenon και μπορεί να σχηματίσει ενώσεις με οξυγόνο, αλλά αυτές είναι γενικά λιγότερο σταθερές.
* ενώσεις αργού: Το Argon έχει βρεθεί ότι σχηματίζει μερικές ασταθείς ενώσεις, όπως το εξαιρετικά αντιδραστικό ARF.
Συνοπτικά: Η έλλειψη αντιδραστικότητας των ευγενών αερίων προέρχεται από το σταθερό, πλήρες εξωτερικό κέλυφος ηλεκτρονίων, την ενέργεια υψηλής ιονισμού και τη χαμηλή συγγένεια ηλεκτρονίων. Είναι πολύ αντιδραστικά υπό τυποποιημένες συνθήκες, αλλά υπάρχουν ορισμένες εξαιρέσεις με τα βαρύτερα ευγενή αέρια, ιδιαίτερα το Xenon και το Radon.