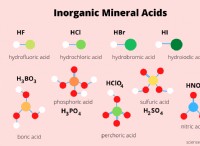
Γιατί θα θέλατε να επιταχύνετε μια χημική αντίδραση;
1. Βιομηχανική παραγωγή:
* Αυξημένη απόδοση: Οι ταχύτερες αντιδράσεις σημαίνουν ότι περισσότερο προϊόν μπορεί να παραχθεί σε λιγότερο χρόνο, οδηγώντας σε μεγαλύτερη αποτελεσματικότητα και εξοικονόμηση κόστους.
* Μειωμένο κόστος: Μια ταχύτερη αντίδραση μπορεί να επιτρέψει χαμηλότερες θερμοκρασίες και πιέσεις λειτουργίας, ενδεχομένως μείωση του ενεργειακού κόστους.
* Βελτιωμένος έλεγχος της διαδικασίας: Η επιτάχυνση μιας αντίδρασης μπορεί να επιτρέψει τον καλύτερο έλεγχο της διαδικασίας, οδηγώντας σε πιο συνεπή και υψηλής ποιότητας προϊόντα.
2. Καθημερινή ζωή:
* Ταχύτερη μαγειρική: Προσθέτουμε θερμότητα σε τρόφιμα για να επιταχύνουν τις χημικές αντιδράσεις που εμπλέκονται στο μαγείρεμα, επιτρέποντάς μας να απολαύσουμε τα γεύματα πιο γρήγορα.
* Ταχύτερη ξήρανση: Χρησιμοποιούμε τη θερμότητα για να επιταχύνετε την εξάτμιση του νερού από ρούχα και άλλα υλικά, οδηγώντας σε ταχύτερους χρόνους ξήρανσης.
* Ταχύτερος καθαρισμός: Πολλά προϊόντα καθαρισμού χρησιμοποιούν χημικά που αντιδρούν γρήγορα για να σπάσουν τη βρωμιά και το βρωμιά, καθιστώντας τον καθαρισμό πιο αποτελεσματικό και αποτελεσματικό.
3. Επιστημονική έρευνα:
* Μελέτες μηχανισμών αντίδρασης: Με τον χειρισμό του ρυθμού αντίδρασης, οι επιστήμονες μπορούν να αποκτήσουν γνώσεις στα λεπτομερή βήματα που εμπλέκονται σε μια χημική αντίδραση.
* Σύνθεση νέων ενώσεων: Οι ταχύτερες αντιδράσεις μπορούν να επιτρέψουν την αποτελεσματική σύνθεση νέων και πολύτιμων ενώσεων, συμβάλλοντας στις εξελίξεις στην ιατρική, στην επιστήμη των υλικών και σε άλλους τομείς.
* Ανάπτυξη νέων καταλυτών: Με την κατανόηση του τρόπου με τον οποίο οι καταλύτες επιταχύνουν τις αντιδράσεις, οι επιστήμονες μπορούν να σχεδιάσουν νέους και αποτελεσματικότερους καταλύτες για συγκεκριμένες διαδικασίες.
4. Ιατρικές εφαρμογές:
* Ανάπτυξη φαρμάκων: Οι ταχύτερες αντιδράσεις μπορούν να οδηγήσουν σε πιο αποτελεσματική σύνθεση φαρμάκων, καθιστώντας τις νέες θεραπείες πιο γρήγορα.
* Ιατρική απεικόνιση: Ορισμένες χημικές αντιδράσεις χρησιμοποιούνται σε τεχνικές ιατρικής απεικόνισης και η επιτάχυνση αυτών των αντιδράσεων μπορεί να βελτιώσει τη σαφήνεια της εικόνας και να μειώσει τους χρόνους σάρωσης.
* Παράδοση φαρμάκου: Ορισμένα συστήματα χορήγησης φαρμάκων βασίζονται σε ελεγχόμενες χημικές αντιδράσεις και η προσαρμογή του ρυθμού αντίδρασης μπορεί να επηρεάσει την απελευθέρωση και την αποτελεσματικότητα του φαρμάκου.
5. Περιβαλλοντικές εφαρμογές:
* θεραπεία αποβλήτων: Οι ταχύτερες αντιδράσεις μπορούν να βοηθήσουν στην καταστροφή των ρύπων πιο αποτελεσματικά, οδηγώντας σε καθαρότερο αέρα και νερό.
* Ανανεώσιμη ενέργεια: Ορισμένες τεχνολογίες ανανεώσιμων πηγών ενέργειας βασίζονται σε χημικές αντιδράσεις και η αύξηση του ρυθμού αντίδρασης μπορεί να οδηγήσει σε αποτελεσματικότερη παραγωγή ενέργειας.
Αυτά είναι μερικά μόνο παραδείγματα γιατί ίσως θέλουμε να επιταχύνουμε μια χημική αντίδραση. Με τον χειρισμό του ρυθμού αντίδρασης, μπορούμε να βελτιώσουμε την αποτελεσματικότητα, να μειώσουμε το κόστος, να αναπτύξουμε νέες τεχνολογίες και να κάνουμε τον κόσμο μια καλύτερη θέση.