Είναι το χλώριο και το ιώδιο φθόριο παρόμοιο με τα ευγενή αέρια;
Εδώ είναι μια κατανομή:
ομοιότητες:
* Όλα είναι μη μέταλλα: Τα αλογόνα και τα ευγενή αέρια είναι και τα δύο μη μέταλλα, που σημαίνει ότι δεν διαθέτουν τις μεταλλικές ιδιότητες στοιχείων όπως ο σιδήρου και ο χαλκός.
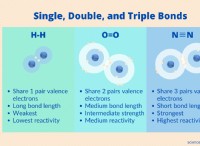
* μπορεί να σχηματίσει διατομικά μόρια: Τόσο τα αλογόνα όσο και τα ευγενή αέρια υπάρχουν ως διατομικά μόρια (δύο άτομα που συνδέονται μαζί) στη στοιχειακή τους μορφή. Για παράδειγμα, το φθόριο (F₂), το χλώριο (CL₂) και το ιώδιο (i₂) είναι διατομικά μόρια.
* Σχετικά χαμηλή αντιδραστικότητα: Τα αλογόνα είναι πιο αντιδραστικά από τα ευγενή αέρια, αλλά εξακολουθούν να είναι λιγότερο αντιδραστικά από τα περισσότερα άλλα στοιχεία. Αυτό οφείλεται στο γεγονός ότι έχουν ένα πλήρες εξωτερικό κέλυφος ηλεκτρονίων, καθιστώντας τα σχετικά σταθερά.
Διαφορές:
* Ηλεκτροργατιστικότητα: Τα αλογόνα έχουν υψηλή ηλεκτροαρνητικότητα, που σημαίνει ότι προσελκύουν έντονα ηλεκτρόνια. Τα ευγενή αέρια έχουν πολύ χαμηλή ηλεκτροαρνητικότητα.
* Αντιδραστικότητα: Τα αλογόνα είναι εξαιρετικά αντιδραστικά, ειδικά φθορίνια, το οποίο είναι το πιο αντιδραστικό στοιχείο στον περιοδικό πίνακα. Τα ευγενή αέρια είναι γενικά μη αντιδραστικά.
* Σχηματισμός ενώσεων: Τα αλογόνα σχηματίζουν εύκολα ενώσεις με άλλα στοιχεία, ιδιαίτερα μέταλλα, για να επιτευχθούν ένα σταθερό οκτάτο. Τα ευγενή αέρια είναι γενικά αδρανή και δεν σχηματίζουν εύκολα ενώσεις.
Συνοπτικά:
Τα αλογόνα και τα ευγενή αέρια είναι και τα δύο μέταλλα με κάποιες ομοιότητες στη συμπεριφορά τους. Ωστόσο, τα αλογόνα είναι σημαντικά πιο αντιδραστικά από τα ευγενή αέρια λόγω της υψηλής ηλεκτροαρνητικότητάς τους και της τάσης να σχηματίζουν ενώσεις.