Ποια είναι η διαφορά μεταξύ Epimers και Anomers;
Τα ανωμερή και τα επιμερή είναι και τα δύο διαστερεομερή, αλλά ένα επιμερές είναι ένα στερεοϊσομερές που διαφέρει στη διαμόρφωση σε οποιοδήποτε μεμονωμένο στερεογονικό κέντρο, ενώ ένα ανωμερές είναι στην πραγματικότητα ένα επιμερές που διαφέρει στη διαμόρφωση στον άνθρακα ακετάλης/ημιακετάλης.
Πριν μιλήσουμε για τις διαφορές μεταξύ των επιμερών και των ανωμερών με περισσότερες λεπτομέρειες, βοηθάει αν καταλάβουμε πρώτα τι είναι τα στερεοϊσομερή.
Τι είναι ένα στερεοϊσομερές;
Προκειμένου να κατανοήσουμε τι είναι ένα στερεοϊσομερές, είναι σημαντικό να γνωρίζουμε ένα ή δύο πράγματα για την ισομέρεια γενικά. Ένα ισομερές είναι ένα μόριο που έχει τον ίδιο μοριακό τύπο με ένα άλλο μόριο, αλλά έχει διαφορετικές χημικές ιδιότητες. Ένας άλλος τρόπος να το πούμε αυτό είναι ότι τα ισομερή περιέχουν τον ίδιο αριθμό ατόμων κάθε στοιχείου, αλλά η διάταξη αυτών των ατόμων είναι διαφορετική.
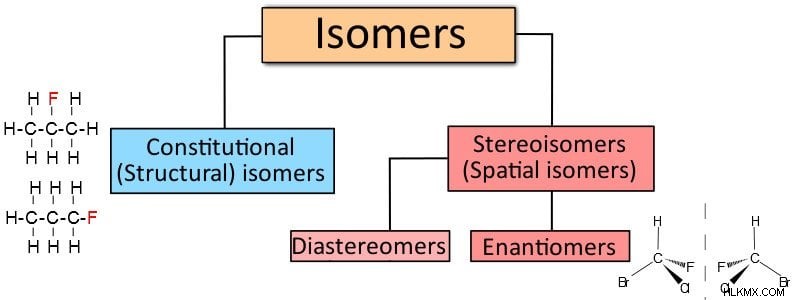
Οι διάφοροι τύποι ισομερών, συμπεριλαμβανομένων των ισομερών θέσης 2-φθοροπροπάνιο και 1-φθοροπροπάνιο στα αριστερά (Προστασία φωτογραφίας :Vladsinger / Wikimedia Commons)
Υπάρχουν δύο είδη ισομερισμού. δομική ισομέρεια (όπου οι λειτουργικές ομάδες συνδέονται με διαφορετικούς τρόπους) και στερεοϊσομέρεια.
Τι είναι ο στερεοϊσομερισμός;
Τα στερεοϊσομερή είναι ισομερή μόρια των οποίων ο μοριακός τύπος είναι ο ίδιος, αλλά οι τρισδιάστατοι προσανατολισμοί των συστατικών τους ατόμων στο διάστημα είναι διαφορετικοί. Τα στερεοϊσομερή χωρίζονται περαιτέρω σε δύο τύπους:εναντιομερή και διαστερεομερή.
Τα εναντιομερή είναι στερεοϊσομερή που είναι μη υπερτιθέμενες κατοπτρικές εικόνες μεταξύ τους. Γνωστά και ως οπτικά ισομερή, αυτά έχουν παρόμοιες φυσικές ιδιότητες.
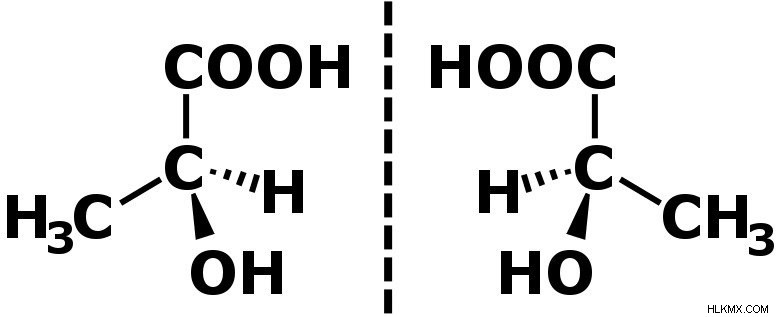
Το (S)-(+)-γαλακτικό οξύ (αριστερά) και το (R)-(-)-γαλακτικό οξύ (δεξιά) είναι κατοπτρικές εικόνες που δεν μπορούν να επικαλεστούν το ένα το άλλο (Πιστωτική φωτογραφία :NEUROtiker / Wikimedia Commons)
Τα διαστερεοϊσομερή είναι εκείνα τα στερεοϊσομερή που έχουν διαφορετικές διαμορφώσεις σε ένα ή περισσότερα (αλλά όχι σε όλα) στερεοϊσομερή χωρίς να είναι κατοπτρικές εικόνες το ένα του άλλου. Ο όρος «επιμερές» χρησιμοποιείται για να αναφέρεται σε διαστερεομερή που διαφέρουν ως προς τη διαμόρφωση σε ένα μόνο χειρικό κέντρο.
Ένα ανωμερές είναι στην πραγματικότητα ένα είδος επιμερούς που διαφέρει στη διαμόρφωση, ειδικά στον άνθρακα ακετάλης/ημιακετάλης.
Epimer vs Anomer
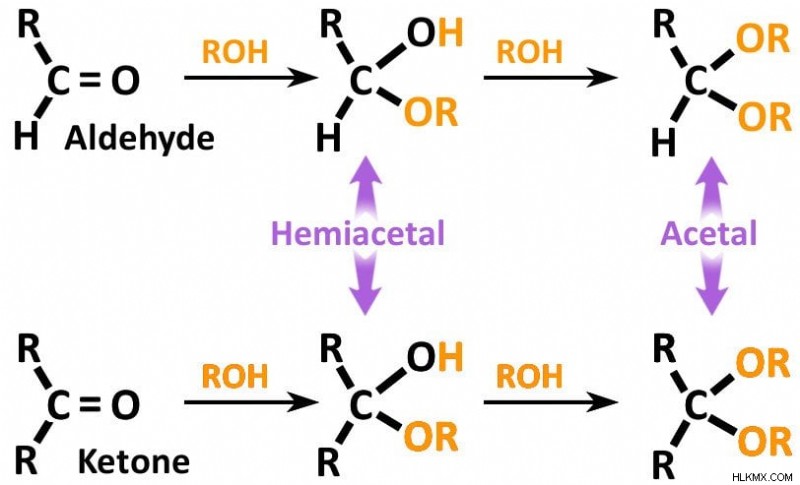
Ενώ ένα επιμερές είναι ένα από ένα ζεύγος στερεοϊσομερών που διαφέρουν ως προς τη διαμόρφωση σε ένα μόνο χειρικό (στερεογενές) κέντρο, ένα ανωμερές είναι στην πραγματικότητα ένα επιμερές (επίσης ένας κυκλικός σακχαρίτης) που διαφέρει στη διαμόρφωση, ειδικά στον άνθρακα ακετάλης ή ημιακετάλης (ανατρέξτε στο την παρακάτω εικόνα για να γίνει διάκριση μεταξύ ακετάλης και ημιακετάλης άνθρακα).
Ένα επιμερές είναι ένα από ένα ζεύγος στερεοϊσομερών που διαφέρουν ως προς τη διαμόρφωση μόνο στο χειρόμορφο κέντρο. Ως εκ τούτου, όλα τα άλλα στερεόκεντρα (αν υπάρχουν) είναι τα ίδια και στα δύο μόρια. Εάν το ζεύγος των μορίων έχει μόνο 1 στερεόκεντρο, τότε τα επιμερή είναι εναντιομερή, ενώ όταν τα μόρια έχουν 2 ή περισσότερα στερεόκεντρα, τα επιμερή αναφέρονται ως διαστερεομερή. (Πηγή)
Ανατρέξτε στην παρακάτω εικόνα με δύο στερεοϊσομερή χλωροβουτάνιου.
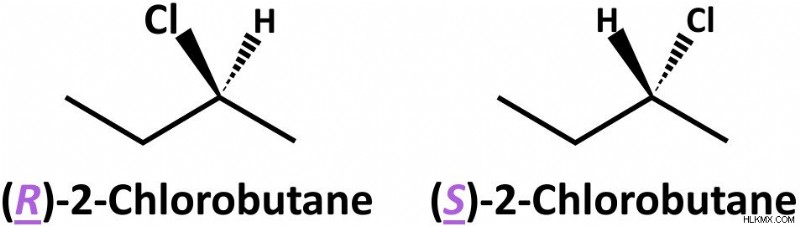
Το (R)-2-χλωροβουτάνιο και το (S)-2-χλωροβουτάνιο διαφέρουν σε απόλυτη διαμόρφωση στο στερεόκεντρο C2. Σημειώστε ότι το 2-χλωροβουτάνιο έχει μόνο ένα στερεόκεντρο. γι' αυτό αυτά τα επιμερή είναι εναντιομερή.
Από την άλλη πλευρά, στις στερεοϊσομερείς δομές του τρυγικού οξέος, μπορείτε να δείτε ότι τα δύο επιμερή (δηλ., (2R,3R)-τρυγικό οξύ και (2R,3S)-τρυγικό οξύ) διαφέρουν στην απόλυτη διαμόρφωση στο στερεόκεντρο C3 .
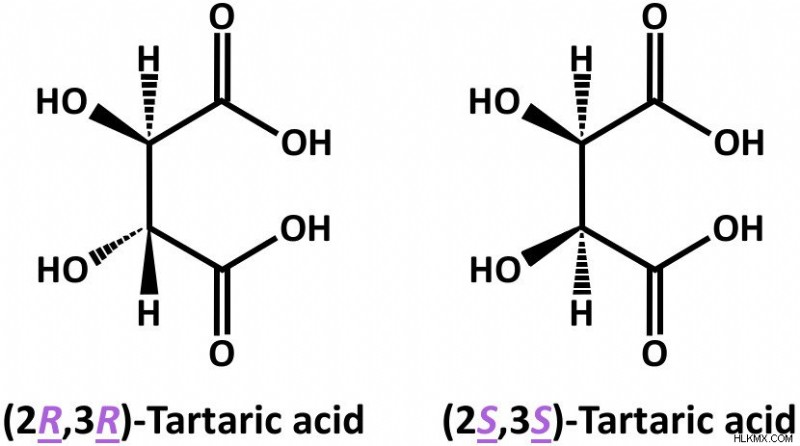
Σημειώστε ότι το τρυγικό οξύ έχει δύο στερεόκεντρα, γι' αυτό και αυτά τα επιμερή είναι διαστερεομερή.
Ένα ανωμερές είναι ένα είδος στερεοϊσομερούς. Τα ανωμερή είναι σακχαρίτες ή γλυκοσίδες που είναι επιμερή, τα οποία είναι διακριτά μεταξύ τους στη διαμόρφωση στο C-2, εάν είναι κετόζες ή στη διαμόρφωση του C-1, εάν είναι αλδόζες.
Σε πολλές περιπτώσεις, οι υδατάνθρακες υπάρχουν σε κυκλικές/άκυκλες μορφές. Κατά τη διάρκεια της κυκλοποίησης, ο άνθρακας στην ομάδα καρβονυλίου μετατρέπεται σε ένα νέο στερεόκεντρο. Μια τέτοια κυκλοποίηση έχει ως αποτέλεσμα τον σχηματισμό δύο διαστερεομερών, τα οποία διαφέρουν ως προς τη θέση σύνδεσης μιας ορισμένης λειτουργικής ομάδας (Πηγή). Το νέο στερεόκεντρο ονομάζεται «ανωμερής άνθρακας».
Το παρακάτω σχήμα θα σας βοηθήσει να το οπτικοποιήσετε:
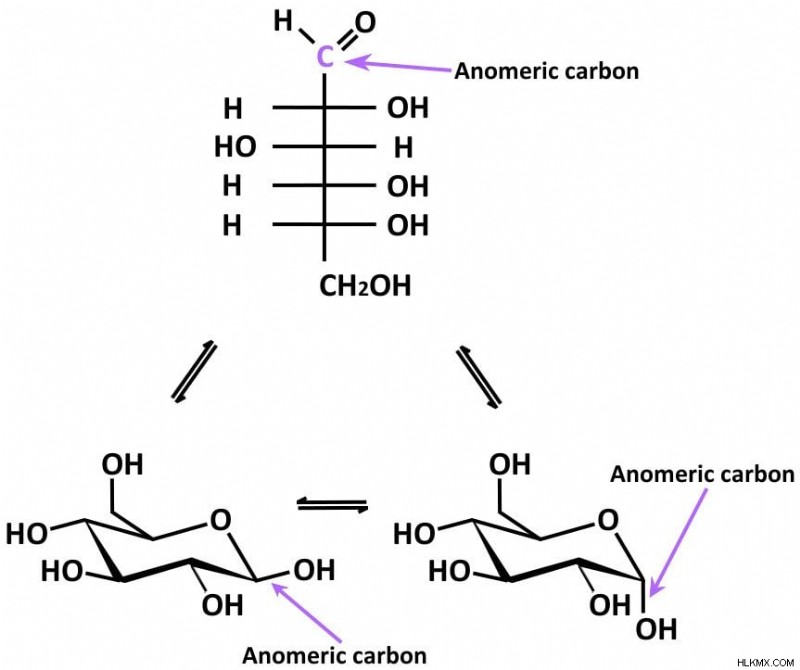
Δύο ανωμερή ορίζονται άλφα και beta, d εξαρτάται από τη σχέση διαμόρφωσης μεταξύ του ανωμερούς κέντρου και του ανωμερούς ατόμου αναφοράς. Εάν η ομάδα υδροξυλίου στο C-1 και η ομάδα -CH2OH στο C5 βρίσκονται στις αντίθετες πλευρές του εξαμελούς δακτυλίου, το C1 λέγεται ότι είναι το ανωμερές α. Εάν βρίσκονται στην ίδια πλευρά, το C1 λέγεται ότι είναι το ανωμερές β.
Παράδειγμα:α-D-γλυκοπυρανόζη και β-D-γλυκοπυρανόζη.
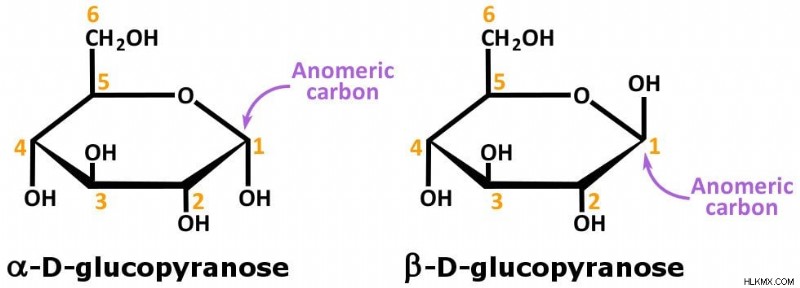
Σημειώστε ότι τα δύο στερεοϊσομερή (στο παραπάνω σχήμα) διαφέρουν μεταξύ τους στη διαμόρφωση του C-1.
Συμπερασματικά, τόσο τα επιμερή όσο και τα ανωμερή είναι στερεοϊσομερή. Στην πραγματικότητα, τα ανωμερή είναι μια ειδική περίπτωση επιμερών. Η κύρια διαφορά μεταξύ τους είναι ότι τα επιμερή διαφέρουν ως προς τη διαμόρφωση μόνο σε ένα χειρόμορφο (στερεογονικό) κέντρο, αλλά τα ανωμερή διαφέρουν ως προς τη διαμόρφωση, ειδικά στον άνθρακα της ακετάλης ή της ημιακετάλης.









