Τι είναι η οξείδωση;
Οξείδωση είναι η διαδικασία κατά την οποία ένα άτομο χάνει ένα ηλεκτρόνιο σε μια αντίδραση με οξυγόνο και νερό. Ένα καστανό μήλο ή ένα σκουριασμένο ποδήλατο είναι κοινά σημεία όπου μπορεί να παρατηρηθεί οξείδωση.
Η οξείδωση είναι ένα κοινό φαινόμενο. ένα καστανό μήλο ή ένα σκουριασμένο ποδήλατο είναι και τα δύο κοινά παραδείγματα αντιδράσεων οξείδωσης. Οξείδωση δεν σημαίνει ότι προστίθεται άτομο οξυγόνου στην ένωση. Αντίθετα, είναι μια χημική αντίδραση που περιλαμβάνει την απώλεια ηλεκτρονίων. Τα μέταλλα γενικά θεωρούνται στοιχεία που μπορούν εύκολα να χάσουν ηλεκτρόνια, επομένως είναι γνωστό ότι οξειδώνονται εύκολα.
Αυτό το χαμένο ηλεκτρόνιο δεν περιφέρεται στο σύμπαν άσκοπα. καταλαμβάνεται από άλλο άτομο. Όταν ένα άτομο δέχεται ένα ηλεκτρόνιο, ονομάζεται αντίδραση αναγωγής . Η οξείδωση και η αναγωγή πάνε χέρι-χέρι και αναφέρονται από κοινού ως αντιδράσεις οξειδοαναγωγής.
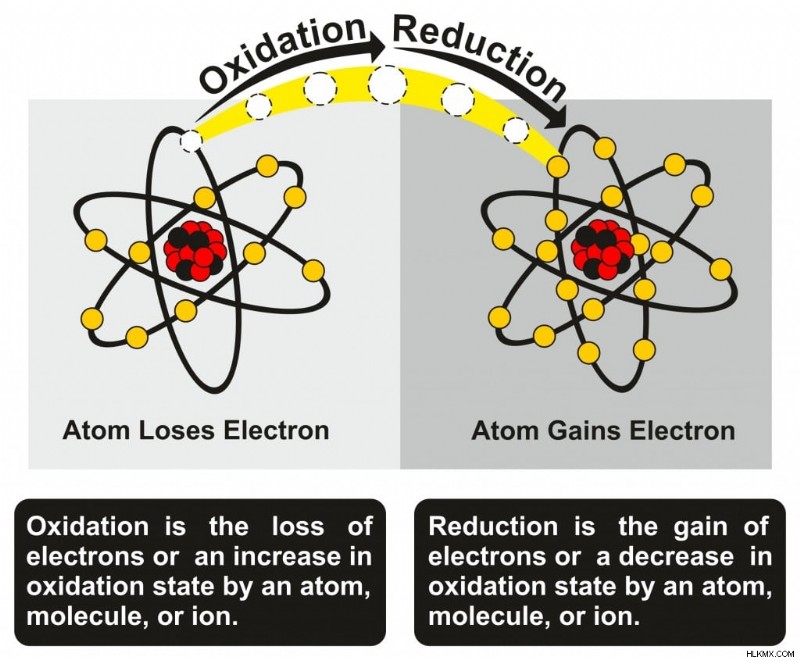
Αντίδραση οξείδωσης και αναγωγής. (Φωτογραφία:udaix/Shutterstock)
Ένας απλός τρόπος για να θυμάστε την οξείδωση και τη μείωση είναι το OIL-RIG. Η οξείδωση είναι η απώλεια ηλεκτρονίων και η αναγωγή είναι η πρόσληψη ηλεκτρονίων. Μπορείτε να με ευχαριστήσετε αργότερα!
Για να διευκολύνουμε τα πράγματα, θα συζητήσουμε μόνο τις αντιδράσεις οξείδωσης σε αυτό το συγκεκριμένο άρθρο.
Τι είναι ένας αριθμός/κατάσταση οξείδωσης;
Ένα άτομο λέγεται ότι οξειδώνεται όταν χάνει ένα ηλεκτρόνιο. Ο αριθμός των ηλεκτρονίων που θα χαθούν εξαρτάται από τον αριθμό οξείδωσης του ατόμου ή του μορίου.
Ο αριθμός οξείδωσης ή η κατάσταση οξείδωσης είναι το φορτίο ενός ατόμου. Μπορεί να είναι θετικό, αρνητικό ή μηδενικό. Οι αριθμοί οξείδωσης δεν αντιστοιχούν πάντα στα πραγματικά φορτία των μορίων.
Ένα άτομο θα έχει αριθμό οξείδωσης μηδέν όταν βρίσκεται στη στοιχειακή του κατάσταση. Αυτή η κατάσταση ενός ατόμου είναι όταν έχει μηδενική διαμόρφωση εδάφους ή είναι σε ουδέτερη κατάσταση. Το νάτριο έχει 11 ηλεκτρόνια. αυτή είναι η μηδενική κατάστασή του. Στη φύση, ο αριθμός οξείδωσης σπάνια είναι μηδέν, καθώς τα άτομα τείνουν πάντα να αποκτούν ή να χάνουν ηλεκτρόνια για να σχηματίσουν ενώσεις.
Ο αριθμός οξείδωσης εξαρτάται από την ηλεκτραρνητικότητα του ατόμου, η οποία προκαθορίζεται από τη θέση του στον περιοδικό πίνακα. Κατά κανόνα, τα στοιχεία στην αριστερή πλευρά του πίνακα είναι λιγότερο ηλεκτραρνητικά και επομένως μπορούν να χάνουν εύκολα ηλεκτρόνια. Ως αποτέλεσμα, έχουν θετικό αριθμό οξείδωσης. Τα στοιχεία της ομάδας Ι συνήθως οξειδώνονται, καθώς χάνουν το ηλεκτρόνιο σθένους τους ενώ σχηματίζουν χημικούς δεσμούς. Ο αριθμός οξείδωσής τους είναι +1. Ένα ηλεκτρόνιο σθένους είναι ένα ηλεκτρόνιο στο εξωτερικό περίβλημα ενός ατόμου.
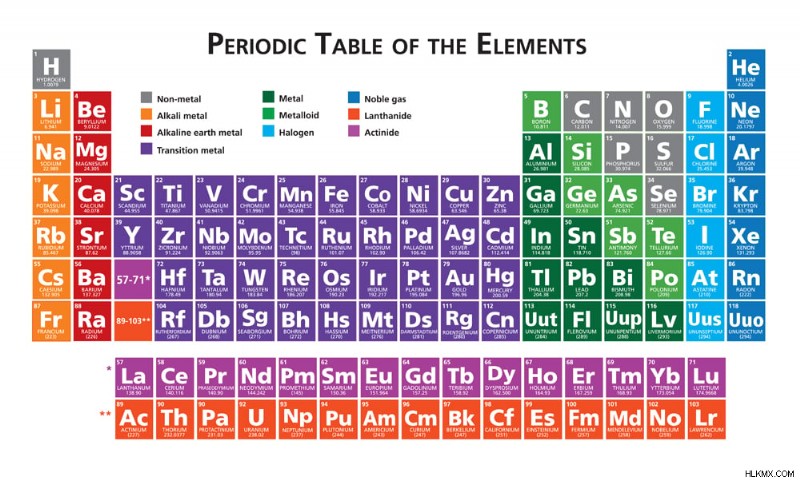
Περιοδικός Πίνακας. (Φωτογραφία:julie deshaies/Shutterstock)
Αυτή η ιδιότητα των στοιχείων αλλάζει καθώς κινούμαστε προς τη δεξιά πλευρά του πίνακα, όπου τα στοιχεία τείνουν να αποκτούν ηλεκτρόνια και έχουν αρνητικό αριθμό οξείδωσης. Πάρτε για παράδειγμα αλογόνα, τα οποία είναι εξαιρετικά ηλεκτραρνητικά και συνήθως υφίστανται αντίδραση αναγωγής. Κερδίζουν ένα ηλεκτρόνιο για να έχουν μια διαμόρφωση παρόμοια με αυτή των ευγενών αερίων. Αυτό τους αφήνει με μια κατάσταση οξείδωσης -1. Ο αριθμός οξείδωσης είναι αρνητικός, καθώς έχουν αποκτήσει 2 ηλεκτρόνια, σε αντίθεση με την απώλεια ηλεκτρονίων.
Όταν πρόκειται για άτομο υδρογόνου, έχει μόνο ένα ηλεκτρόνιο στη μηδενική διαμόρφωση του και μπορεί είτε να κερδίσει είτε να χάσει ένα ηλεκτρόνιο. Αυτό δίνει στο υδρογόνο μια κατάσταση οξείδωσης +1 ή -1. Το άτομο υδρογόνου μπορεί να είναι αναγωγικός ή οξειδωτικός παράγοντας, ανάλογα με το στοιχείο με το οποίο αλληλεπιδρά.
Τι είναι ένας οξειδωτικός και ένας αναγωγικός παράγοντας;
Οξειδωτικός παράγοντας είναι μια ουσία που οξειδώνει άλλες ουσίες. Αυτό σημαίνει ότι επιτρέπει σε άλλη ουσία να υποστεί οξείδωση. Για να διασπαστεί ακόμη περισσότερο, όταν υπάρχει ένας οξειδωτικός παράγοντας σε μια αντίδραση, προκαλεί άλλα άτομα στην αντίδραση να χάσουν ένα ηλεκτρόνιο. Αυτά τα χαμένα ηλεκτρόνια γίνονται αποδεκτά από τον οξειδωτικό παράγοντα. Ως αποτέλεσμα, οι οξειδωτικοί παράγοντες ονομάζονται δέκτες ηλεκτρονίων .
Αυτό είναι όπως όταν προσλαμβάνετε κάποιον για να κάνει κάποια δουλειά και να αφαιρέσει μέρος του φορτίου από τους ώμους σας. Αυτός ο εξωτερικός πράκτορας αφαιρεί το βάρος της εργασίας από εσάς, ενώ στη διαδικασία καταπονείται.
Με άλλα λόγια, ένας αναγωγικός παράγοντας είναι μια ουσία που βοηθά άλλες ουσίες να μειωθούν σε μια αντίδραση. Ο αναγωγικός παράγοντας βοηθά την ουσία να αποκτήσει ένα ηλεκτρόνιο.
Ένα άτομο που αποκτά ένα ηλεκτρόνιο ονομάζεται οξειδωτικός παράγοντας , καθώς επιτρέπει στο άλλο άτομο να χάσει το ηλεκτρόνιο και να υποστεί οξείδωση. Από την άλλη πλευρά, ένα άτομο που χάνει ένα ηλεκτρόνιο είναι αναγωγικός παράγοντας, καθώς επιτρέπει στο άλλο άτομο να αποκτήσει ένα ηλεκτρόνιο και να υποστεί αναγωγή.
Σκεφτείτε ξανά τη συντομογραφία OIL-RIG. Χωρίς αυτή τη θεμελιώδη κατανόηση, θα είναι δύσκολο να κατανοήσουμε πλήρως τη διαδικασία.
Πώς σκουριάζει ο σίδηρος;
Η σκουριά, ή το οξείδιο του σιδήρου, είναι το πιο κοινό παράδειγμα οξείδωσης. Το γυαλιστερό μέταλλο (σίδηρος) αναπτύσσει ένα καφέ στρώμα κατά την αντίδραση με το οξυγόνο και το νερό. Η αντίδραση είναι ταχύτερη στο θαλασσινό νερό, καθώς το αλάτι τείνει να διαβρώνει το μέταλλο γρήγορα. Αυτό οφείλεται σε ηλεκτροχημικές αντιδράσεις, όπου πραγματοποιείται μεταφορά ηλεκτρονίων μεταξύ 2 ουσιών—ενός στερεού και ενός υγρού.
Η σκουριά δεν εμφανίζεται στον ξηρό αέρα, αλλά αντίθετα εμφανίζεται όταν ο αέρας συνοδεύεται από νερό. Η υγρασία είναι ένας σημαντικός παράγοντας για τη σκουριά του σιδήρου.
Η απλή αντίδραση είναι:
Σίδηρος + νερό + οξυγόνο Ενυδατωμένο οξείδιο του σιδήρου
Πιο συγκεκριμένα, η αντίδραση είναι η εξής:
2Fe2+ + 4OH– → 2Fe(OH)2 (υδροξείδιο σιδήρου)
Η αντίδραση περιλαμβάνει ένα ιόν σιδήρου και το ιόν υδροξειδίου (υδρογόνο και οξυγόνο), το οποίο αντιδρά για να μας δώσει υδροξείδιο του σιδήρου.
Αυτό το υδροξείδιο του σιδήρου αντιδρά περαιτέρω με το οξυγόνο για να δώσει σκουριά, Fe2O3.
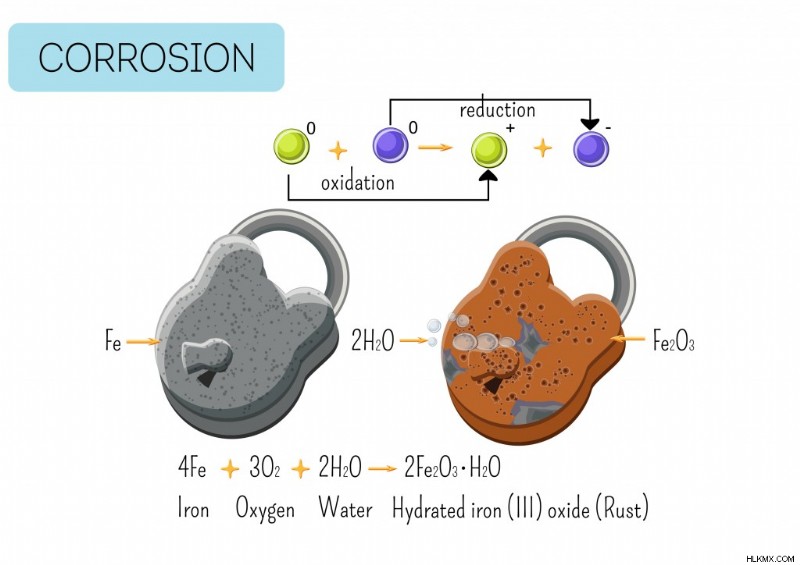
Διάβρωση του σιδήρου όταν εκτίθεται σε νερό και οξυγόνο. (Φωτογραφία:Inna Bigun/Shutterstock)
Τόσο το ελεύθερο αέριο οξυγόνο (O2) όσο και το διοξείδιο του άνθρακα (CO2) που υπάρχουν στον αέρα μπορούν να αποτελέσουν πηγή οξυγόνου για το σχηματισμό σκουριάς. Μόλις εγκατασταθεί η σκουριά, το μέταλλο αρχίζει να υποβαθμίζεται περαιτέρω, και τελικά γίνεται εύθραυστο και ακατάλληλο για χρήση.
Συμπέρασμα
Ενώ μπορεί να είναι καιρός να πούμε αντίο σε ένα παλιό σκουριασμένο ποδήλατο, υπάρχει ακόμα ελπίδα για άλλα μεταλλικά αντικείμενα. Το καντράν του ρολογιού σας, για παράδειγμα, είναι κατασκευασμένο από ανοξείδωτο ατσάλι και σπάνια θα έχει την ίδια μοίρα με ένα ποδήλατο. Ο ανοξείδωτος χάλυβας αποτρέπει τη διάβρωση των αντικειμένων, καθώς διαχωρίζει την επιφάνεια του μετάλλου από τον αέρα και το νερό, επιτρέποντάς του να διαρκέσει για πολλά χρόνια.
Ο ανοξείδωτος χάλυβας είναι ένα κράμα, που σημαίνει ότι είναι ένας συνδυασμός μετάλλων, μαζί με διάφορα άλλα στοιχεία. Αποτελείται από σίδηρο, χρώμιο, μαγγάνιο, πυρίτιο, άνθρακα και σε ορισμένες περιπτώσεις, μικρές ποσότητες νικελίου και μολυβδαινίου. Αυτά τα στοιχεία αντιδρούν με το οξυγόνο παρουσία νερού για να σχηματίσουν ένα λεπτό και σταθερό φιλμ. Το φιλμ αποτρέπει τη διάβρωση δημιουργώντας ένα φράγμα στον αέρα και το νερό.
Η οξείδωση δεν είναι κακό, απλώς ένας ανεπιθύμητος επισκέπτης που είναι δύσκολο να εξαλειφθεί. Ευτυχώς, η σωστή φροντίδα των μεταλλικών αντικειμένων μπορεί να βοηθήσει στην πρόληψη ή την επιβράδυνση της οξείδωσης. Η εφαρμογή λιπαντικού ή προστατευτικής επικάλυψης μπορεί να βοηθήσει, αν και αυτή δεν είναι αλάνθαστη μέθοδος.
Δεν μπορείτε να ξεφύγετε από την επίδραση των οξειδωτικών αντιδράσεων που συμβαίνουν στη φύση. η μόνη διέξοδος είναι η λήψη προληπτικών μέτρων για την καθυστέρηση της εμφάνισής τους ή τον μετριασμό της εξάπλωσής τους!




