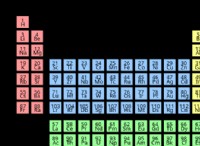
Ηλεκτρονική Διαμόρφωση Ακτινιδών
Η σειρά ακτινιδών είναι η στοιχειακή σειρά στην τελευταία σειρά του περιοδικού πίνακα με ατομικούς αριθμούς από το 89 έως το 103.
Αυτά τα στοιχεία είναι ραδιενεργά και έχουν μεγάλο εύρος αριθμών οξείδωσης.
Το ουράνιο είναι το πιο κοινό και γνωστό στοιχείο. Χρησιμοποιείται ως πυρηνικό καύσιμο όταν υφίσταται πυρηνική αντίδραση και μετατρέπεται σε πλουτώνιο.
Τα στοιχεία της σειράς ακτινιδών είναι ραδιενεργά, πράγμα που σημαίνει ότι εκπέμπουν πολλή ενέργεια κατά τη διάρκεια της ραδιενεργής διάσπασης.
Το ουράνιο και το θόριο είναι οι πιο άφθονες ακτινίδες που υπάρχουν στη Γη, ενώ το πλουτώνιο συντίθεται.
Ηλεκτρονική διαμόρφωση ακτινιδών
Η ακτινίδη είναι ένα στοιχείο που καταλαμβάνει την 5η τροχιά της (n2)ης τροχιάς και ονομάζεται επίσης στοιχείο μπλοκ 5f.
Και τα 15 συστατικά των ακτινιδών ξεκινώντας από το Ac89 (5f0 6d1 7s2 ) έως το Lr103 (5f14 6d1 7s2) ταξινομούνται σε αυτή τη σειρά, καθώς όλα έχουν πανομοιότυπα απτά και χαρακτηριστικά σύνθεσης.
Αυτό συμβαίνει επειδή το ακτίνιο θεωρείται μια έκδοση των ακτινιδών.
Οι ακτινίδες έχουν τη γενική ηλεκτρονική διαμόρφωση [Rn] 5f0-14 6d0-1 7s2. Επειδή η διαφορά ενέργειας μεταξύ 5f και 6d είναι ασήμαντη, είναι δύσκολο να εκτιμηθεί εάν τα ηλεκτρόνια έχουν εισέλθει στο τροχιακό 5f ή 6d.
Οι ακτινίδες είναι η δεύτερη σειρά στοιχείων f-block. Με ηλεκτρονική διαμόρφωση [Rn] 5f1-14 6d 0-17s2, όπου Rn είναι η ηλεκτρονική διαμόρφωση του πλησιέστερου ευγενούς αερίου, δηλαδή του Ραδίου.
Επειδή οι ενέργειες των ηλεκτρονίων στα τροχιακά 5f και 6d είναι κοντά, τα ηλεκτρόνια μετακινούνται στο τροχιακό 5f.
Τα 14 ηλεκτρόνια άλλων στοιχείων, εκτός από το Θόριο, προστίθενται στο τροχιακό 5f. Αυτές οι ανωμαλίες στην ηλεκτρονική διαμόρφωση της ακτινίδης προκύπτουν από τη σταθερότητα των επιβατών f0, f7 και f14 των τροχιακών 5f.
Τα ηλεκτρόνια στο τροχιακό 5f μπορούν επίσης να συνδεθούν σε μεγαλύτερο βαθμό.
Στοιχειακός πίνακας
Το σθένος, όπως φαίνεται στις αναφερόμενες διατάξεις των στοιχείων ακτινιδών, είναι η ηλεκτρονική διάταξη του ακτινίου [Rn]5f0 6d1 7s2. Μετά από αυτό είναι οι δεκατέσσερις ακτινίδες, το τελευταίο υποατομικό σωματίδιο που θα εισέλθει στο υποκέλυφος 6d.
Το επιπλέον υποατομικό σωματίδιο θα πρέπει να εισέλθει σε ένα 5fsub-shell στο επόμενο στοιχείο, Th. Και αυτή η διαδικασία πρέπει να επαναληφθεί μέχρι το τελικό στοιχείο, Lr.
Σαν αποτέλεσμα, το 6d υποκέλυφος σε κάθε στοιχείο πρέπει να παραμείνει γεμάτο χωριστά, αποδίδοντας το αναμενόμενο σθένος των διατάξεων κελύφους 5f1-146d1 7s2 για αυτά τα στοιχεία.
Η ενέργεια των υπο-κελυφών (6d&5f) είναι σχεδόν πανομοιότυπη και τα στοιχεία των ατομικών σειρών είναι απίστευτα περίπλοκα. Η αναγνώριση του τροχιακού σύμφωνα με τον αριθμό των πρωτονίων και των νετρονίων για την καταγραφή των διατάξεων είναι δύσκολη.
Το σθένος των ηλεκτρονικών διατάξεων του κελύφους των στοιχείων είναι πολύ σημαντικό για τη χημική απόδοση. Επιπλέον, ο ανταγωνιστικός παράγοντας μεταξύ 5fn 6d0 7s2 και 5fn-16d1 7s2 είναι μοναδικός.
Οι ηλεκτρονικές διαμορφώσεις των ακτινιδών δεν τηρούν τη βασική συμπεριφορά όπως οι λανθανίδες. Λόγω των σχεδόν ίσων ενεργειών των 5f και 6d, τα ηλεκτρόνια στα 4 αρχικά στοιχεία ακτινιδών, το Ακτίνιο, το Θόριο, το Πρωτακτίνιο και το Ουράνιο, μπορεί να καταλαμβάνουν τα υποκέλυφα 5f ή 6d ή και τα δύο.
Εκτός από τα Cm (Z=96) και Lr (Z=103), όπου το ηλεκτρόνιο 6d1 δεν μετατοπίζεται στο 5f λόγω σταθερών διαμορφώσεων 5f7 και 5f14, 6d1 ηλεκτρόνιο μετατοπίζεται στο 5f-υποφλοιό από Pu (Z=94).
Παρά το γεγονός ότι ανήκει στη σειρά 5f, είναι σαφές ότι ο Th στερείται f-ηλεκτρονίου (δηλ. ακτινίδες), όπου τόσο οι αναμενόμενες όσο και οι πραγματικές διαμορφώσεις του Pa, Τα U, Np, Cm και Lr είναι τα ίδια. Σε αντίθεση με άλλες ακτινίδες, το 6d-υποφλοιό δεν διαθέτει d-ηλεκτρόνιο.
Κατάσταση οξείδωσης
Οι ακτινίδες έχουν διαφορετικές καταστάσεις οξείδωσης λόγω της χαμηλότερης διαφοράς ενέργειας μεταξύ των τροχιακών 5f, 6d και 7s.
Αν και το 3+ είναι η πιο σταθερή κατάσταση οξείδωσης, είναι δυνατές πρόσθετες καταστάσεις οξείδωσης λόγω της ισχυρής θωράκισης των f-ηλεκτρονίων.
Η μέγιστη δυνατή κατάσταση οξείδωσης αυξάνεται μέχρι το μέσο της σειράς και στη συνέχεια πέφτει, δηλ. από +4 για Th σε +5, +6 και +7 για Pa, V και Np, στη μέση.
Συμπέρασμα
Οι ακτινίδες έχουν ραδιενεργές ιδιότητες μαζί με πολλή ενέργεια. Διαθέτουν επίσης υψηλότερη χημική αντιδραστικότητα και χαμηλότερες ενθαλπίες ιονισμού.
Οι ακτινίδες έχουν ηλεκτρονική διαμόρφωση 7s2, με παραλλαγές στα υποκέλυφα 5f και 6f. Καθώς ο πίνακας προχωρά από το Th στο Lr, τα ατομικά και ιοντικά μεγέθη των στοιχείων μειώνονται.
Σχετικές σελίδες| Ειδοποιήσεις JEE | Υλικό μελέτης JEE |
| Διαφορά μεταξύ JEE | Σημαντικές φόρμουλες JEE |
| Συμβουλές για τις εξετάσεις JEE | Πλήρες φόρμες JEE |
| Μέσες τετραγωνικές ταχύτητες ρίζας | Τύπος ακτινωτών και γωνιακών κόμβων |
| Μαγνητικές ιδιότητες των στοιχείων d-Block | Περιορισμοί της θεωρίας του Arrhenius |
| Η εξίσωση Nernst και οι εφαρμογές της | Θεωρίες γαλακτωματοποίησης |