Χημικοί δεσμοί
Όλα τα ζωντανά όντα αποτελούνται από άτομα και αλληλεπιδρούν μεταξύ τους για να σχηματίσουν μόρια. Τα άτομα στα μόρια συγκρατούνται μεταξύ τους με χημικούς δεσμούς και ως εκ τούτου συμπεριφέρονται σαν μια ενιαία οντότητα. Λόγω της μεταβλητής αντοχής των δεσμών, βοηθά στη συγκράτηση των μορίων μέσα σε ένα συστατικό. Η σημασία του χημικού δεσμού παρατηρείται σε όλους τους ζωντανούς οργανισμούς για διάφορες ρυθμιστικές και μεταβολικές λειτουργίες. Υπάρχουν διάφοροι τύποι χημικών δεσμών και καθένας από αυτούς έχει τις ιδιότητές του. Το άρθρο εξετάζει λεπτομερώς τους δεσμούς και τον τρόπο με τον οποίο συγκρατούν τα άτομα.
Σχηματισμός χημικών δεσμών μεταξύ ατόμων
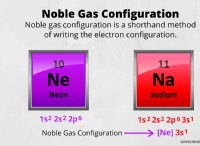
Τα άτομα ενώνονται και σχηματίζουν διάφορους τύπους χημικών δεσμών λόγω της ηλεκτροστατικής έλξης μεταξύ των ηλεκτρονίων που είναι αρνητικά φορτισμένα και θετικά φορτισμένα πρωτόνια. Η δύναμη έλξης που συνδυάζει δύο ή περισσότερα άτομα σχηματίζει τους δεσμούς. Όταν τα άτομα έρχονται κοντά το ένα στο άλλο, ο χημικός δεσμός σχηματίζεται λόγω της ανακατανομής των ηλεκτρονίων. Ως εκ τούτου, ο δεσμός βοηθά στην απόκτηση σταθερής ηλεκτρονικής διαμόρφωσης που οδηγεί στη σταθεροποίηση των συνδεδεμένων μορίων. Ακολουθούν οι τρόποι με τους οποίους σχηματίζονται οι χημικοί δεσμοί μεταξύ των ατόμων:
- Όταν ένα άτομο χάνει ένα ή περισσότερα ηλεκτρόνια από ένα άλλο άτομο
- Όταν ένα άτομο αποκτά ένα ή περισσότερα ηλεκτρόνια σε ένα άλλο άτομο
- Όταν μοιράζονται ηλεκτρόνια μεταξύ των ατόμων
Κύριοι τύποι χημικών δεσμών
Η αλληλεπίδραση μεταξύ δύο ή περισσότερων ατόμων οδηγεί σε διάφορους τύπους δεσμών. Ακολουθούν οι τύποι των χημικών δεσμών που οφείλονται σε συνένωση των ατόμων:
- Ιονικός δεσμός – Όταν ένα άτομο γίνεται πιο σταθερό χάνοντας ή κερδίζοντας ένα ηλεκτρόνιο, οδηγεί στο σχηματισμό ενός ιόντος που είναι ένα φορτισμένο σωματίδιο. Τα κατιόντα είναι θετικά ιόντα που σχηματίζονται λόγω απώλειας ηλεκτρονίων, ενώ τα ανιόντα είναι αρνητικά ιόντα που σχηματίζονται λόγω της απόκτησης ηλεκτρονίων. Αυτοί οι δεσμοί σχηματίζονται μεταξύ ενός μετάλλου και ενός μη μετάλλου λόγω της πλήρους μεταφοράς ενός ή περισσότερων ηλεκτρονίων από το ένα άτομο στο άλλο. Αυτά σχηματίζονται μεταξύ ιόντων διαφορετικών φορτίων. Ένα παράδειγμα περιλαμβάνει το NaCl, όπου το Na και το Cl συνδυάζονται με νάτριο δίνοντας ένα ηλεκτρόνιο ενώ το χλώριο το δέχεται.
- Ομοιοπολικός δεσμός – Σε αυτόν τον χημικό δεσμό, ο δεσμός μεταξύ δύο ατόμων ενισχύεται με την κοινή χρήση των ηλεκτρονίων. Σε αυτόν τον τύπο δεσμού, τα άτομα μοιράζονται τα ηλεκτρόνια μόνο από τον εξωτερικό δακτύλιο με ένα άλλο άτομο. Εμφανίζεται κυρίως μεταξύ μη μεταλλικών ουσιών. Ένα παράδειγμα είναι το νερό (H2O), όπου το υδρογόνο και το οξυγόνο σχηματίζουν δεσμό μοιράζοντας ηλεκτρόνια. Οι ομοιοπολικοί δεσμοί είναι δύο τύπων.
Οι πολικοί ομοιοπολικοί δεσμοί είναι όταν τα ηλεκτρόνια μοιράζονται άνισα τα άτομα, γεγονός που οδηγεί στην ανάπτυξη ελαφρώς θετικών και ελαφρώς αρνητικών φορτίων σε διαφορετικά μέρη του μορίου.
Μη πολικοί ομοιοπολικοί δεσμοί είναι εκείνοι στους οποίους οι δεσμοί σχηματίζονται μεταξύ δύο ατόμων του ίδιου ή διαφορετικών στοιχείων και τα ηλεκτρόνια μοιράζονται εξίσου.
- Δεσμός Υδρογόνου – Πρόκειται για χημικούς δεσμούς στους οποίους το άτομο υδρογόνου ενός μορίου σχηματίζει δεσμό με το ηλεκτραρνητικό άτομο ενός άλλου μορίου. Οδηγεί στο σχηματισμό διπολικών αποτελεσμάτων λόγω της ισχυρής έλξης του ατόμου του υδρογόνου προς το ηλεκτραρνητικό άτομο.
Από τους τρεις χημικούς δεσμούς, ο ισχυρός είναι ο ομοιοπολικός δεσμός, καθώς σε αυτόν, ο δεσμός σχηματίζεται μεταξύ δύο ατόμων λόγω της αμοιβαίας κοινής χρήσης ηλεκτρονίων. Ο ιοντικός δεσμός ακολουθεί αυτό και ο πιο αδύναμος είναι ο δεσμός υδρογόνου επειδή είναι εύκολο να σπάσει ο δεσμός που δημιουργείται μεταξύ του ατόμου του υδρογόνου και του ηλεκτραρνητικού ατόμου ενός άλλου μορίου.
Οι χημικοί δεσμοί είναι σημαντικοί με διάφορους τρόπους
Οι χημικοί δεσμοί είναι σημαντικοί για τους ζωντανούς οργανισμούς καθώς βοηθούν στη δημιουργία σταθερότητας και είναι ζωτικής σημασίας για τη συνολική ρυθμιστική και μεταβολική λειτουργικότητα. Οι δεσμοί είναι σημαντικοί για τη συγκέντρωση ατόμων και το σχηματισμό μορίων.
- Οι χημικοί δεσμοί είναι ζωτικής σημασίας για την επιβίωση των ζωντανών μορφών, καθώς βοηθούν στη διαχείριση της συνολικής ανθρώπινης φυσιολογίας. Καθώς τα άτομα συγκρατούνται μεταξύ τους με τη βοήθεια των δεσμών, βοηθά στην ομοιόσταση, την κυτταρική σηματοδότηση και τη λειτουργία πολλών βιολογικών διεργασιών.
- Η σημασία του χημικού δεσμού είναι ακόμη σημαντική στην παρασκευή φαρμάκων και, ως εκ τούτου, είναι μια σημαντική πτυχή της χημείας.
- Οι δεσμοί υδρογόνου συγκρατούν δύο κλώνους DNA στη διπλή έλικα και, ως εκ τούτου, είναι σημαντικός στη γενετική.
- Το NaCl είναι ένα παράδειγμα ενός ομοιοπολικού δεσμού που είναι το αλάτι, και ως εκ τούτου λειτουργεί ως ηλεκτρολύτης που είναι σημαντικός για διάφορες ρυθμίσεις στο σώμα.
Συμπέρασμα
Το άρθρο δίνει μια βασική εισαγωγή στους χημικούς δεσμούς, στους διάφορους τύπους και στο πώς σχηματίζεται κάθε δεσμός. Ο δεσμός σχηματίζεται είτε μοιράζοντας τα ηλεκτρόνια, κερδίζοντας ή χάνοντας ένα ηλεκτρόνιο σε άλλο άτομο, είτε σχηματίζοντας έναν δεσμό του μορίου υδρογόνου με ένα ηλεκτραρνητικό άτομο άλλου μορίου. Οι πιο κοινές μορφές χημικών δεσμών περιλαμβάνουν ομοιοπολικούς, ιοντικούς και υδρογόνους δεσμούς. Οι ομοιοπολικοί δεσμοί είναι ισχυρότεροι καθώς σχηματίζονται λόγω της αμοιβαίας κοινής χρήσης των ηλεκτρονίων και ως εκ τούτου σταθεροποιεί τον δεσμό μεταξύ των ατόμων. Η σημασία των χημικών δεσμών εντοπίζεται σε διάφορες φυσιολογικές διεργασίες σε ζωντανούς οργανισμούς και σε διάφορες συνθετικές παραγωγές.