Τι συμβαίνει με τα σωματίδια σε ένα άλας καθώς διαλύουν το νερό;
1. Η πολικότητα έχει σημασία:
* αλάτι (NaCl): Το αλάτι είναι μια ιοντική ένωση, που σημαίνει ότι αποτελείται από θετικά φορτισμένα ιόντα νατρίου (Na+) και αρνητικά φορτισμένα ιόντα χλωριούχου (Cl-). Αυτά τα ιόντα συγκρατούνται από ισχυρές ηλεκτροστατικές δυνάμεις.
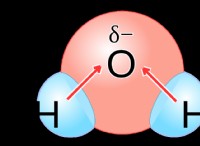
* νερό (H2O): Το νερό είναι ένα πολικό μόριο, που σημαίνει ότι έχει ένα ελαφρώς θετικό άκρο (κοντά στα άτομα υδρογόνου) και ένα ελαφρώς αρνητικό άκρο (κοντά στο άτομο οξυγόνου). Αυτή η πολικότητα επιτρέπει στα μόρια του νερού να αλληλεπιδρούν με φορτισμένα σωματίδια.
2. Ενυδάτωση:
* έλξη: Το θετικό άκρο των μορίων νερού (υδρογόνο) προσελκύεται από τα αρνητικά φορτισμένα ιόντα χλωριούχου (Cl-) στο αλάτι. Ομοίως, το αρνητικό τέλος των μορίων νερού (οξυγόνο) προσελκύεται από τα θετικά φορτισμένα ιόντα νατρίου (Na+).
* περιβάλλον: Αυτά τα αξιοθέατα προκαλούν τη συσσώρευση μορίων νερού γύρω από τα ιόντα αλατιού. Αυτή η διαδικασία ονομάζεται ενυδάτωση .
* Breaking Bonds: Τα ισχυρά αξιοθέατα μεταξύ των μορίων του νερού και των ιόντων αλατιού ξεπερνούν τις ηλεκτροστατικές δυνάμεις που συγκρατούν το κρύσταλλο αλατιού μαζί. Αυτό προκαλεί τη διάσπαση του κρυστάλλου αλατιού.
3. Διάλυση:
* Διασπορά: Μόλις ο κρύσταλλος του αλατιού σπάσει, τα ατομικά ιόντα νατρίου και χλωριούχου περιβάλλονται από μόρια νερού. Τώρα διασκορπίζονται σε όλο το νερό, διαλύοντας αποτελεσματικά.
4. Λύση:
* ομοιογενές μίγμα: Το προκύπτον μίγμα νερού και διαλυμένων ιόντων άλατος είναι ένα ομοιογενές μίγμα, που σημαίνει ότι έχει μια ομοιόμορφη σύνθεση σε όλη την έκταση.
ουσιαστικά: Η διάλυση του άλατος στο νερό περιλαμβάνει μόρια νερού που απομακρύνουν τα ιόντα αλατιού μέσω ισχυρών αξιοθέατων, δημιουργώντας ένα ομοιογενές μίγμα όπου τα ιόντα κατανέμονται ομοιόμορφα.