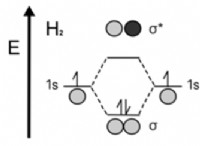
Τι σας λέει ένας σύνθετος τύπος;
1. Ταυτότητα: Προσδιορίζει τα στοιχεία που υπάρχουν στην ένωση. Για παράδειγμα, το H₂O μας λέει ότι το νερό περιέχει υδρογόνο (Η) και οξυγόνο (Ο).
2. Αναλογία: Υποδεικνύει τον σχετικό αριθμό ατόμων κάθε στοιχείου στην ένωση. Οι δείκτες στον τύπο αντιπροσωπεύουν αυτήν την αναλογία. Για παράδειγμα, το H₂o μας λέει ότι υπάρχουν δύο άτομα υδρογόνου για κάθε άτομο οξυγόνου.
3. Μοριακό βάρος: Χρησιμοποιώντας τα ατομικά βάρη των στοιχείων, μπορείτε να υπολογίσετε το μοριακό βάρος της ένωσης. Αυτό βοηθά στον προσδιορισμό της μάζας ενός μόνο μορίου.
4. Εμπειρική φόρμουλα: Ο σύνθετος τύπος μπορεί επίσης να εκφραστεί ως εμπειρική φόρμουλα, η οποία αντιπροσωπεύει τον απλούστερο λόγο ατόμων ατόμων στην ένωση. Για παράδειγμα, η εμπειρική φόρμουλα για τη γλυκόζη (c₆h₁₂o₆) είναι ch₂o.
5. Δομικές πληροφορίες: Μερικές φορές, ο τύπος μπορεί να παρέχει ορισμένες δομικές πληροφορίες. Για παράδειγμα, ένας τύπος όπως το ch₃cooh προτείνει την παρουσία μιας ομάδας καρβοξυλικού οξέος. Ωστόσο, για λεπτομερείς δομικές πληροφορίες, χρειάζεστε μια δομική φόρμουλα.
Συνοπτικά, ένας σύνθετος τύπος παρέχει πληροφορίες σχετικά με τα παρόντα στοιχεία, τη σχετική τους αφθονία και τη συνολική σύνθεση της ένωσης. Είναι ένας συνοπτικός τρόπος να αντιπροσωπεύουμε τη χημική μακιγιάζ μιας ουσίας.