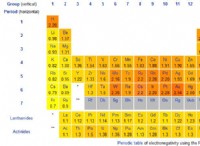
Είναι η ευκολία και η ταχύτητα με την οποία ένα στοιχείο συνδυάζει άλλες ουσίες;
Εδώ είναι μια κατανομή:
* Αντιδραστικότητα: Ένα μέτρο για το πόσο εύκολα ένα στοιχείο υφίσταται χημικές αντιδράσεις.
* ευκολία: Αναφέρεται στην τάση ενός στοιχείου να συμμετέχει σε χημικές αντιδράσεις. Ορισμένα στοιχεία αντιδρούν εύκολα, ενώ άλλα είναι λιγότερο αντιδραστικά.
* ταχύτητα: Αναφέρεται στον ρυθμό με τον οποίο εμφανίζεται μια χημική αντίδραση. Τα εξαιρετικά αντιδραστικά στοιχεία τείνουν να αντιδρούν γρήγορα, ενώ τα λιγότερα αντιδραστικά στοιχεία μπορούν να αντιδράσουν αργά ή καθόλου.
Παράγοντες που επηρεάζουν την αντιδραστικότητα:
* Διαμόρφωση ηλεκτρονίων: Η διάταξη των ηλεκτρονίων στα άτομα ενός στοιχείου καθορίζει την τάση του να κερδίζει, να χάνει ή να μοιράζεται ηλεκτρόνια, γεγονός που οδηγεί σε χημικές αντιδράσεις.
* Ηλεκτροργατιστικότητα: Η ικανότητα ενός ατόμου να προσελκύει ηλεκτρόνια σε χημικό δεσμό. Περισσότερα ηλεκτροαρνητικά στοιχεία τείνουν να είναι πιο αντιδραστικά.
* ενέργεια ιονισμού: Η ενέργεια που απαιτείται για την απομάκρυνση ενός ηλεκτρονίου από ένα άτομο. Στοιχεία με χαμηλές ενέργειες ιονισμού είναι πιο πιθανό να χάσουν ηλεκτρόνια και να αντιδρούν.
* Ατομικό μέγεθος: Τα μεγαλύτερα άτομα έχουν γενικά ασθενέστερα αξιοθέατα στα εξωτερικά τους ηλεκτρόνια, καθιστώντας τα πιο αντιδραστικά.
Παραδείγματα:
* νάτριο (na) είναι εξαιρετικά αντιδραστικό επειδή χάνει εύκολα το εξώτατο ηλεκτρόνιο του για να σχηματίσει ένα θετικό ιόν.
* χρυσό (au) είναι πολύ αντιδραστικό επειδή τα ηλεκτρόνια του είναι στενά διατηρούνται και είναι δύσκολο να τα αφαιρέσετε.
Η κατανόηση της αντιδραστικότητας είναι ζωτικής σημασίας στη χημεία, καθώς μας βοηθά να προβλέψουμε πώς θα συμπεριφέρονται τα στοιχεία σε διάφορα χημικά περιβάλλοντα.