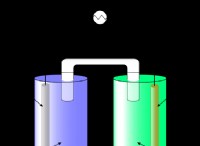
Τα άτομα νατρίου και χλωρίου συνδυάζονται εύκολα επειδή και οι δύο τείνουν να χάνουν ηλεκτρόνια.
* νάτριο (na) έχει ένα μόνο ηλεκτρόνιο στο εξώτατο κέλυφος του. Τείνει να χάσει Αυτό το ηλεκτρόνιο για να επιτευχθεί ένα σταθερό, πλήρες εξωτερικό κέλυφος, σχηματίζοντας ένα θετικά φορτισμένο ιόν νατρίου (Na+).
* χλώριο (cl) έχει επτά ηλεκτρόνια στο εξωτερικό κέλυφος του. Τείνει να κερδίζει ένα ηλεκτρόνιο για να επιτευχθεί ένα σταθερό, πλήρες εξωτερικό κέλυφος, σχηματίζοντας ένα αρνητικά φορτισμένο χλωριούχο ιόν (Cl-).
Ο συνδυασμός νατρίου και χλωρίου οδηγείται από τις αντίθετες τάσεις των δύο ατόμων:
* Το νάτριο θέλει να χάσει * ένα ηλεκτρόνιο.
* Το χλώριο θέλει να κερδίσει * ένα ηλεκτρόνιο.
Η ηλεκτροστατική έλξη μεταξύ του θετικά φορτισμένου ιόντος νατρίου και του αρνητικά φορτισμένου χλωριούχου ιόντος είναι αυτό που σχηματίζει τον ιονικό δεσμό στο χλωριούχο νάτριο (NaCl), κοινώς γνωστό ως επιτραπέζιο αλάτι.