Είναι το υδροξείδιο το ίδιο με το υπεροξείδιο;
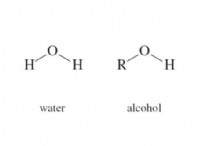
Υδροξείδιο (OH-)
* Ορισμός: Ένα αρνητικά φορτισμένο πολυατομικό ιόν που αποτελείται από ένα άτομο οξυγόνου και ένα άτομο υδρογόνου.
* Ιδιότητες:
* Ισχυρή βάση
* Βρέθηκε σε πολλές ανόργανες και οργανικές ενώσεις
* Υπεύθυνος για την αλκαλικότητα των λύσεων
* Παραδείγματα: Υδροξείδιο νατρίου (NaOH), υδροξείδιο του καλίου (ΚΟΗ)
υπεροξείδιο (o2^2-)
* Ορισμός: Ένα αρνητικά φορτισμένο πολυατομικό ιόν που αποτελείται από δύο άτομα οξυγόνου που συνδέονται μαζί με έναν μόνο δεσμό.
* Ιδιότητες:
* Ισχυρός παράγοντας οξειδωτικής
* Μπορεί να αποσυντεθεί σε οξυγόνο και νερό
* Χρησιμοποιείται ως πράκτορας λεύκανσης και απολυμαντικό
* Παραδείγματα: Υπεροξείδιο του υδρογόνου (H2O2), υπεροξείδιο του νατρίου (Na2O2)
Βασικές διαφορές:
* Σύνθεση: Το υδροξείδιο έχει ένα άτομο οξυγόνου και ένα άτομο υδρογόνου, ενώ το υπεροξείδιο έχει δύο άτομα οξυγόνου.
* Δομή: Το υδροξείδιο είναι γραμμικό, ενώ το υπεροξείδιο είναι λυγισμένο.
* Χημικές ιδιότητες: Το υδροξείδιο είναι μια ισχυρή βάση, ενώ το υπεροξείδιο είναι ένας ισχυρός οξειδωτικός παράγοντας.
Συνοπτικά, το υδροξείδιο και το υπεροξείδιο είναι ξεχωριστά χημικά είδη με διαφορετικές συνθέσεις, δομές και ιδιότητες. Δεν πρέπει να θεωρούνται τα ίδια.