Ορισμός χημικού τύπου και παραδείγματα
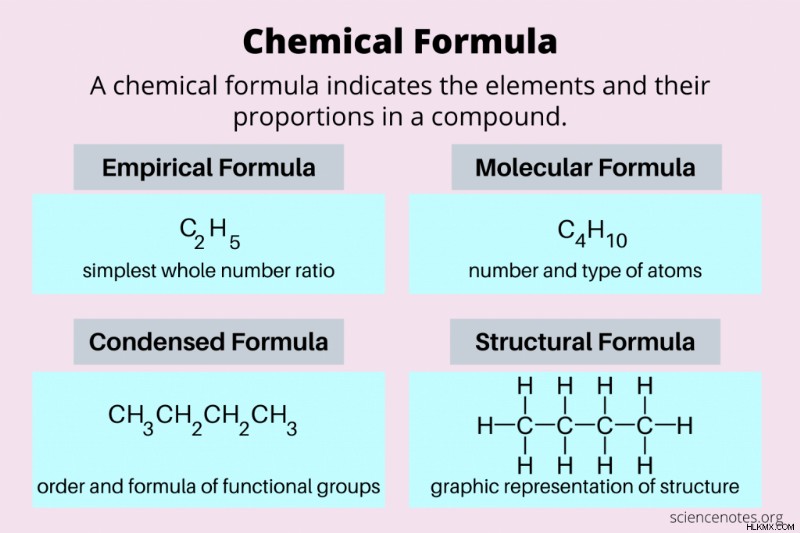
Ένας χημικός τύπος είναι συμβολισμός που δείχνει τον αριθμό και τον τύπο των ατόμων σε ένα μόριο. Με άλλα λόγια, είναι μια γραπτή αναπαράσταση ενός τρισδιάστατου αντικειμένου. Υπάρχουν μερικοί διαφορετικοί τρόποι γραφής ενός χημικού τύπου. Γενικά, ένας τύπος περιλαμβάνει σύμβολα στοιχείων που προσδιορίζουν τους τύπους των ατόμων στο μόριο. Στους περισσότερους τύπους, οι δείκτες που ακολουθούν ένα σύμβολο στοιχείου υποδεικνύουν τον αριθμό των ατόμων αυτού του στοιχείου.
Ακολουθεί μια ματιά στους πιο συνηθισμένους τύπους χημικών τύπων:εμπειρικούς τύπους, μοριακούς τύπους, συμπυκνωμένους τύπους και δομικούς τύπους.
| Χημικός τύπος | Περιγραφή | Παράδειγμα (βουτάνιο) |
|---|---|---|
| Εμπειρικός τύπος | απλός ακέραιος λόγος στοιχείων | C2 H5 |
| Μοριακός τύπος | αριθμός και τύπος ατόμων στο πραγματικό μόριο | C4 H10 |
| Δομικός τύπος | δισδιάστατη αναπαράσταση τρισδιάστατης δομής | CH3 CH2 CH2 CH3 |
Μέρη ενός χημικού τύπου
- Σύμβολα στοιχείων :Γράψτε το σύμβολο ενός ή δύο γραμμάτων για κάθε στοιχείο. Για παράδειγμα, το σύμβολο για το υδρογόνο είναι H. Το σύμβολο για το χρυσό είναι Au.
- Σειρά συμβόλων :Κατά σύμβαση, το κατιόν ή το θετικό μέρος του μορίου πηγαίνει πρώτο, ακολουθούμενο από το ανιόν ή το αρνητικό μέρος του μορίου. Για παράδειγμα, γράφετε H2 O αντί για O2 H.
- Συντελεστής :Ένας συντελεστής είναι ο αριθμός που γράφεται πριν από έναν τύπο. Εάν υπάρχει, υποδεικνύει τον αριθμό των μορίων.
- Συνδρομή :Ένας δείκτης είναι ένας αριθμός που γράφεται μετά από ένα σύμβολο στοιχείου που υποδεικνύει τον αριθμό των ατόμων αυτού του στοιχείου. Για παράδειγμα, το "2" στο H2 O σημαίνει ότι κάθε μόριο νερού έχει δύο άτομα υδρογόνου. Ο αριθμός "1" δεν γράφεται. Έτσι, κάθε μόριο νερού περιέχει ένα άτομο οξυγόνου.
- Εκθέτης :Ένας εκθέτης είναι ένας αριθμός που γράφεται πάνω από έναν τύπο και στα δεξιά του. Υποδεικνύει καθαρό ηλεκτρικό φορτίο. Ο αριθμός παραλείπεται για μία μόνο χρέωση. Για παράδειγμα, γράψτε OH και όχι OH. Όταν υπάρχει, ο αριθμός προηγείται της χρέωσης. Για παράδειγμα, γράψτε SO4 .
Εμπειρικός τύπος
Ο εμπειρικός τύπος δείχνει τη μικρότερη αναλογία ακέραιου αριθμού στοιχείων σε ένα μόριο. Ένα άλλο όνομα για τον εμπειρικό τύπο είναι ο απλούστερος τύπος. Αν και ο εμπειρικός τύπος δεν σας λέει ακριβώς πόσα άτομα κάθε στοιχείου είναι σε ένα μόριο, υποδεικνύει τη μοριακή αναλογία των στοιχείων.
Μοριακός τύπος
Ο μοριακός τύπος είναι αυτό που εννοούν οι περισσότεροι όταν μιλούν για έναν χημικό τύπο. Αυτός είναι ο τύπος που χρησιμοποιείτε όταν γράφετε χημικές εξισώσεις ή παραγγέλνετε χημικά. Ο μοριακός τύπος δίνει τον αριθμό και τον τύπο των ατόμων στο μόριο. Μερικές φορές ο εμπειρικός τύπος και ο μοριακός τύπος είναι ο ίδιος. Για παράδειγμα, H2 Το O είναι τόσο ο εμπειρικός όσο και ο μοριακός τύπος του νερού. Στα πολύπλοκα μόρια, ο εμπειρικός και ο μοριακός τύπος συχνά διαφέρουν. Για παράδειγμα, ο εμπειρικός τύπος του βουτανίου είναι C2 H5 , ενώ ο μοριακός τύπος είναι C4 H10 . Οι δείκτες σε έναν μοριακό τύπο είναι πάντα πολλαπλάσιοι αυτών στον εμπειρικό τύπο.
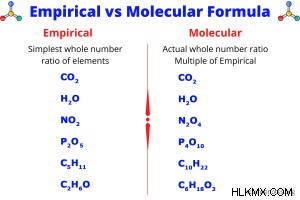
Γσυγκρίνοντας εμπειρικούς και μοριακούς τύπους
Δείτε πώς χρησιμοποιείτε αυτούς τους τύπους σε υπολογισμούς χημείας.
Συμπυκνωμένη φόρμουλα
Ο συμπυκνωμένος τύπος είναι ένας τύπος δομικού τύπου που δείχνει τις λειτουργικές ομάδες σε ένα μόριο. Όπως ένας μοριακός τύπος, περιλαμβάνει τόσο τις ταυτότητες όσο και τους αριθμούς των ατόμων. Για παράδειγμα, ο συμπυκνωμένος τύπος για το βουτάνιο είναι CH3 CH2 CH2 CH3 . Μόλις κοιτάξετε τον τύπο, βλέπετε ότι υπάρχει μια αλυσίδα ατόμων άνθρακα με άτομα υδρογόνου συνδεδεμένα σε αυτά.
Υπάρχει επίσης μια συντομότερη εκδοχή του συμπυκνωμένου τύπου που συμπτύσσει πανομοιότυπες ομάδες. Για παράδειγμα, μπορείτε να γράψετε τον ίδιο τύπο για το βουτάνιο με το CH3 (CH2 )2 CH3 . Αυτό είναι χρήσιμο για την περιγραφή πολυμερών και άλλων μεγάλων μορίων.
Δομικός τύπος
Ένας δομικός τύπος είναι μια δισδιάστατη γραφική αναπαράσταση ενός τρισδιάστατου μορίου. Έτσι, είναι το είδος του τύπου που μπορείτε να σχεδιάσετε, αλλά όχι να πληκτρολογήσετε σε ένα πληκτρολόγιο. Η εξαίρεση είναι ο συμπυκνωμένος τύπος, ο οποίος είναι ένα είδος δομικού τύπου που υποδεικνύει τη θέση των λειτουργικών ομάδων.
Υπάρχουν περισσότερα από ένα είδη δομικών τύπων:
- Συμπυκνωμένη φόρμουλα
- Δομή κουκκίδων Lewis
- Σκελετική φόρμουλα
- Προβολή Newman
- Προβολή αλόγων
- Προβολή Haworth
- Προβολή Fischer
Ένας δομικός τύπος χρησιμοποιεί σύμβολα στοιχείων, αλλά μπορεί να περιλαμβάνει ή να μην περιλαμβάνει δείκτες. Ένας σκελετικός τύπος παραλείπει ακόμη και τα περισσότερα σύμβολα στοιχείων, καθώς οι γραμμές και ο τρόπος που συνδέονται υποδεικνύουν άτομα άνθρακα και υδρογόνου.
Όλοι οι δομικοί τύποι έχουν αντίστοιχους εμπειρικούς και μοριακούς τύπους. Ωστόσο, οι περισσότεροι χημικοί χρησιμοποιούν τον δομικό τύπο όταν περιγράφουν μια χημική αντίδραση επειδή διευκολύνει την οπτικοποίηση της διαδικασίας.
Αναφορές
- Burrows, Andrew. (20131). Χημεία:Εισαγωγή της ανόργανης, οργανικής και φυσικής χημείας (2η έκδ.). Οξφόρδη. ISBN 978-0-19-969185-2.
- Chai, Yan; Guo, Ting; Jin, Changming; et al. (1991). «Φουλερένια με μέταλλα μέσα». Journal of Physical Chemistry . 95 (20):7564–7568. doi:10.1021/j100173a002
- Hill, Edwin A. (1900). «Σε ένα σύστημα ευρετηρίασης της χημικής βιβλιογραφίας. Εγκρίθηκε από το Τμήμα Ταξινόμησης του Γραφείου Ευρεσιτεχνιών των ΗΠΑ». J. Είμαι. Chem. Soc . 22 (8):478–494. doi:10.1021/ja02046a005
- Petrucci, Ralph H.; Harwood, William S.; Herring, F. Geoffrey (2002). Γενική Χημεία:Αρχές και Σύγχρονες Εφαρμογές (8η έκδ.). Upper Saddle River, N.J:Prentice Hall. ISBN 978-0-13-014329-7.