Το χλωριούχο ασβέστιο τήκεται στον πάγο μια χημική ή φυσική αλλαγή;
* Δεν σχηματίζονται νέες ουσίες: Όταν το χλωριούχο ασβέστιο (CaCl₂) προστίθεται στον πάγο, μειώνει το σημείο κατάψυξης του νερού. Ο πάγος λιώνει σε υγρό νερό, αλλά τα ίδια τα μόρια ασβεστίου και το νερό παραμένουν αμετάβλητα.
* Η αλλαγή είναι αναστρέψιμη: Εάν επρόκειτο να παγώσετε το προκύπτον διάλυμα αλμυρού νερού, θα πάρετε πίσω τον πάγο και το χλωριούχο ασβέστιο.
Εδώ συμβαίνει:
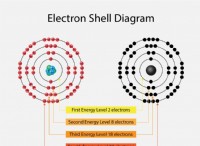
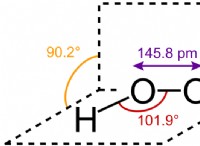
Το χλωριούχο ασβέστιο είναι ένα άλας που διαλύεται εύκολα στο νερό. Όταν διαλύεται, απελευθερώνει ιόντα (Ca2⁺ και CL⁻) που διαταράσσουν τους δεσμούς υδρογόνου που συγκρατούν τα μόρια του νερού μαζί στο πλέγμα πάγου. Αυτή η διαταραχή μειώνει το σημείο κατάψυξης του νερού, προκαλώντας την τήξη του πάγου.
Key Takeaway: Η μεταβολή της κατάστασης από πάγο σε υγρό νερό είναι μια φυσική αλλαγή επειδή η χημική σύνθεση των εμπλεκόμενων ουσιών παραμένει η ίδια.