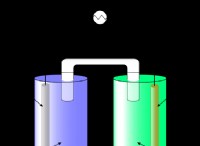
Γιατί ο χαλκός δεν μπορεί να αντικαταστήσει το σίδηρο από το διάλυμα αλατιού του;
Εδώ είναι μια κατανομή:
* Η σειρά αντιδραστικότητας: Τα μέταλλα είναι διατεταγμένα σε μια σειρά αντιδραστικότητας με βάση την τάση τους να χάσουν ηλεκτρόνια. Τα μέταλλα υψηλότερα στη σειρά είναι πιο δραστικά. Ο σίδηρος είναι υψηλότερος στη σειρά από το χαλκό.
* Αντιδράσεις μετατόπισης: Σε μια αντίδραση μετατόπισης, ένα πιο δραστικό μέταλλο μετατοπίζει ένα λιγότερο αντιδραστικό μέταλλο από το διάλυμα αλατιού του.
* Χαλκός και σίδηρος: Όταν ο χαλκός προστίθεται σε διάλυμα σιδήρου, ο χαλκός δεν μπορεί να μετατοπίσει το σίδερο επειδή είναι λιγότερο αντιδραστικό. Δεν έχει την απαραίτητη "κινητήρια δύναμη" για να σπρώξει το σίδερο έξω από τη λύση.
Παράδειγμα: Εάν προσθέσετε ένα κομμάτι χαλκού σε ένα διάλυμα θειικού σιδήρου (II) (FESO₄), τίποτα δεν θα συμβεί. Ο χαλκός δεν θα αντιδράσει και το διάλυμα θα παραμείνει πράσινο (το χρώμα των ιόντων Fe2).
Σε αντίθεση: Εάν προσθέσετε ένα κομμάτι σιδήρου σε διάλυμα θειικού χαλκού (II) (CUSO₄), θα παρατηρήσετε μια αντίδραση. Ο σίδηρος θα μετατοπίσει χαλκό, σχηματίζοντας θειικό σίδηρο (II) και εναπόθεση χαλκού μετάλλου στο σίδηρο:
Fe (s) + cuso₄ (aq) → feso₄ (aq) + cu (s)
Το διάλυμα θα αλλάξει από το μπλε (το χρώμα των ιόντων Cu² ⁺) σε πράσινο ως σχηματισμό θειικού σιδήρου (II).