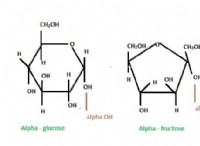
Τι είναι το πιο πολικό άλας ή ζάχαρη;
* ιονική εναντίον ομοιοπολικών δεσμών: Το αλάτι σχηματίζεται από ιοντικούς δεσμούς, που σημαίνει ότι τα ηλεκτρόνια μεταφέρονται πλήρως από το άτομο νατρίου στο άτομο χλωρίου. Αυτό δημιουργεί αντίθετα φορτισμένα ιόντα (Na+ και Cl-), τα οποία προσελκύουν έντονα ο ένας τον άλλον.
* πολικοί ομοιοπολικοί δεσμοί: Η ζάχαρη, από την άλλη πλευρά, συγκρατείται από ομοιοπολικούς δεσμούς. Ενώ αυτοί οι δεσμοί περιλαμβάνουν την κοινή χρήση ηλεκτρονίων, η κοινή χρήση δεν είναι ίση. Τα άτομα οξυγόνου στη ζάχαρη είναι πιο ηλεκτροαρνητικά, τραβώντας τα κοινά ηλεκτρόνια πιο κοντά στον εαυτό τους. Αυτό δημιουργεί μερικές θετικές χρεώσεις στα άτομα άνθρακα και υδρογόνου και μερικές αρνητικές χρεώσεις στα άτομα οξυγόνου.
* πολικότητα: Η διαφορά στην ηλεκτροαρνητικότητα μεταξύ νατρίου και χλωρίου στο άλας δημιουργεί μια πολύ ισχυρή και μόνιμη διπολική στιγμή, καθιστώντας την ιδιαίτερα πολική. Οι μερικές χρεώσεις στη ζάχαρη, ενώ είναι παρόντες, είναι λιγότερο έντονες και λιγότερο μόνιμες λόγω της κοινόχρηστης ηλεκτρονικής φύσης των ομοιοπολικών δεσμών.
Συνοπτικά: Οι ιοντικοί δεσμοί του Salt έχουν ως αποτέλεσμα μια ισχυρή, μόνιμη διπολική στιγμή, καθιστώντας την πιο πολική από τους πολικούς ομοιοπολικούς δεσμούς της ζάχαρης.