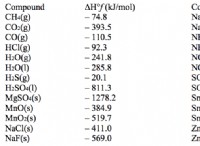
Τι συμβαίνει όταν το NAHCO3 αντιδρά με αιθανοϊκό οξύ;
* Αιθανοϊκό νάτριο (ch₃coona) , επίσης γνωστό ως οξικό νάτριο.
* νερό (h₂o)
* Διοξείδιο του άνθρακα (CO₂) Αέριο
Εδώ είναι η ισορροπημένη χημική εξίσωση:
nahco₃ (aq) + ch₃cooh (aq) → ch₃coona (aq) + h₂o (l) + co₂ (g)
Επεξήγηση:
* Το αιθοϊκό οξύ (οξικό οξύ) είναι ένα αδύναμο οξύ, δωρίζοντας ένα πρωτόνιο (Η) στο ιόν διττανθρακικού άλατος (Hco₃⁻) σε διττανθρακικό νάτριο.
* Το ιόν διττανθρακικού αποδέχεται το πρωτόνιο, σχηματίζοντας ανθρακικό οξύ (H₂co₃).
* Το καρβονικό οξύ είναι ασταθές και αποσυντίθεται εύκολα σε νερό (H₂O) και διοξείδιο του άνθρακα (Co₂).
* Το υπόλοιπο ιόν νατρίου (Na⁺) συνδυάζεται με το ιόν αιθανοϊκό (ch₃coo⁻) για να σχηματίσει αιθοϊκό νατρίου.
Παρατηρήσεις:
* Θα παρατηρήσετε την αναβρασμό (φυσαλίδες) λόγω της απελευθέρωσης αερίου διοξειδίου του άνθρακα.
* Το διάλυμα θα γίνει λιγότερο όξινο καθώς καταναλώνεται το αιθοϊκό οξύ.
* Εάν συνεχίσετε να προσθέτετε διττανθρακικό νάτριο, το διάλυμα τελικά θα γίνει ελαφρώς βασικό λόγω της παρουσίας αιθοειδούς νατρίου, το οποίο είναι το άλας ενός ασθενούς οξέος και μιας ισχυρής βάσης.
Εφαρμογές:
Αυτή η αντίδραση χρησιμοποιείται συνήθως σε:
* ψήσιμο: Το διττανθρακικό νάτριο είναι ένας συνηθισμένος παράγοντας λυγμού στο ψήσιμο, όπου αντιδρά με όξινα συστατικά όπως το βουτυρόγαλα ή το ξύδι για την παραγωγή αερίου διοξειδίου του άνθρακα, το οποίο δημιουργεί τσέπες αέρα και βοηθά στην άνοδο της ζύμης.
* Αντοξίδια: Το διττανθρακικό νάτριο χρησιμοποιείται σε αντιόξινα για την εξουδετέρωση του οξέος του στομάχου.
* Πειράματα χημείας: Αυτή η αντίδραση είναι μια κλασική επίδειξη αντιδράσεων βάσης οξέος και εξέλιξης αερίου.