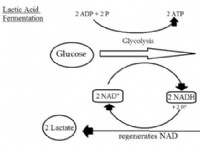
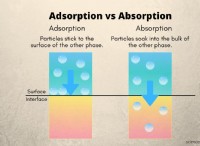
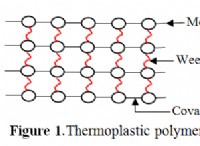
Ποιες μορφές όταν δύο μη μέταλλα μοιράζονται ηλεκτρόνια;
Εδώ είναι γιατί:
* Μη μέταλλα Έχετε την τάση να κερδίζετε ηλεκτρόνια για να επιτύχετε μια σταθερή διαμόρφωση ηλεκτρονίων.
* Κοινή χρήση ηλεκτρονίων Επιτρέπει και στα δύο μέταλλα να φτάσουν σε μια σταθερή κατάσταση χωρίς να χάσουν ή να κερδίζουν ηλεκτρόνια εντελώς.
Αυτή η κοινή χρήση έχει ως αποτέλεσμα ένα ομοιοπολικό δεσμό όπου τα κοινόχρηστα ηλεκτρόνια προσελκύονται από τους πυρήνες και των δύο ατόμων, κρατώντας τα μαζί σε ένα μόριο.
Παραδείγματα ομοιοπολικών δεσμών:
* νερό (h₂o): Το υδρογόνο (Η) και το οξυγόνο (O) μοιράζονται ηλεκτρόνια.
* διοξείδιο του άνθρακα (CO₂): Ο άνθρακας (C) και το οξυγόνο (O) μοιράζονται ηλεκτρόνια.
* Αέριο αζώτου (n₂): Δύο άτομα αζώτου (N) μοιράζονται ηλεκτρόνια.