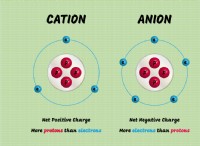
Τι είδους μορφές δεσμών όταν ένα ή περισσότερα ηλεκτρόνια μεταφέρονται από το άτομο σε άλλο που αλλάζει και τα δύο άτομα σε ιόντα;
Εδώ είναι γιατί:
* Μεταφορά ηλεκτρονίων: Το καθοριστικό χαρακτηριστικό της ιοντικής σύνδεσης είναι η πλήρης μεταφορά ηλεκτρονίων από το ένα άτομο στο άλλο.
* Σχηματισμός ιόντων: Το άτομο που χάνει ηλεκτρόνια γίνεται ένα θετικά φορτισμένο ιόν (κατιόν), ενώ το άτομο που κερδίζει ηλεκτρόνια γίνεται ένα αρνητικά φορτισμένο ιόν (ανιόν).
* Ηλεκτροστατική έλξη: Τα αντίθετα φορτία των προκύπτουσων ιόντων δημιουργούν μια ισχυρή ηλεκτροστατική έλξη που τα συγκρατεί σε μια δομή κρυσταλλικού πλέγματος.
Παράδειγμα:
Το νάτριο (Na) έχει ένα ηλεκτρόνιο σθένους, ενώ το χλώριο (CL) έχει επτά. Όταν το νάτριο αντιδρά με χλώριο, το νάτριο χάνει το ηλεκτρόνιο σθένους του σε χλώριο, σχηματίζοντας ένα ιόν νατρίου (Na+) και ένα ιόν χλωριούχου (Cl-). Αυτά τα ιόντα συγκρατούνται από έναν ιοντικό δεσμό, σχηματίζοντας το χλωριούχο νάτριο ένωσης (NaCl), κοινώς γνωστό ως επιτραπέζιο αλάτι.