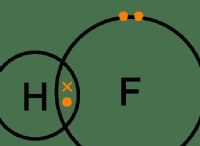
Τι είναι το υδροχλωρικό οξύ;
Υδροχλωρικό οξύ:ένα ισχυρό οξύ
Το υδροχλωρικό οξύ (HCl) είναι ένα ισχυρό, διαβρωτικό οξύ Αυτό βρίσκεται φυσικά στο στομάχι, όπου βοηθά στην πέψη. Ακολουθεί μια ανάλυση των βασικών χαρακτηριστικών της:
Ιδιότητες:
* Χημικός τύπος: HCl
* εμφάνιση: Καθαρό, άχρωμο υγρό με έντονη, ερεθιστική οσμή
* Διαλυτότητα: Αναμίξιμο με νερό
* ph: Πολύ όξινο, με pH 0
* Corrosive: Μπορεί να προκαλέσει σοβαρά εγκαύματα στο δέρμα και τα μάτια
* αντιδραστική: Αντιδρά έντονα με μέταλλα, ανθρακικά και βάσεις
χρησιμοποιεί:
* πέψη: Ως μέρος του γαστρικού χυμού, βοηθά στη διάσπαση των τροφίμων στο στομάχι.
* Βιομηχανική: Χρησιμοποιείται για την κατασκευή διαφόρων προϊόντων, συμπεριλαμβανομένων των πλαστικών, των βαφών και των λιπασμάτων.
* Καθαρισμός: Αποτελεσματική για την αφαίρεση της σκουριάς, του ασβέστη και άλλων καταθέσεων.
* Χημική σύνθεση: Σημαντικό σε πολλές χημικές αντιδράσεις και διαδικασίες.
* Ιατρική: Που χρησιμοποιούνται σε ορισμένα φάρμακα και για τη θεραπεία ορισμένων ιατρικών καταστάσεων.
Ασφάλεια:
* πολύ διαβρωτικό: Το χειρισμό απαιτεί κατάλληλα προστατευτικά εργαλεία, συμπεριλαμβανομένων των γαντιών, των γυαλιών και ενός παλτό εργαστηρίου.
* επιβλαβή εάν απορροφηθεί: Μπορεί να προκαλέσει σοβαρές εγκαύματα στο στόμα, το λαιμό και το στομάχι.
* εισπνοή: Οι αναθυμιάσεις μπορούν να ερεθίσουν το αναπνευστικό σύστημα.
* Αποθήκευση: Αποθηκεύστε σε ένα δροσερό, ξηρό μέρος, μακριά από τη θερμότητα και κατευθύνετε το φως του ήλιου.
Συμπερασματικά:
Το υδροχλωρικό οξύ είναι ένα ισχυρό χημικό με πολυάριθμες εφαρμογές. Ωστόσο, είναι σημαντικό να το χειριστείτε με εξαιρετική προσοχή λόγω της διαβρωτικής φύσης του. Πάντα να ακολουθείτε τις οδηγίες ασφαλείας και να τις αποθηκεύσετε σωστά για να αποφύγετε ατυχήματα.