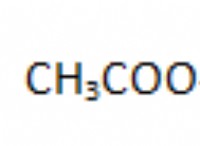Τι συμβαίνει με το σημείο βρασμού μετά το αλάτι διαλύεται στο νερό;
Εδώ είναι γιατί:
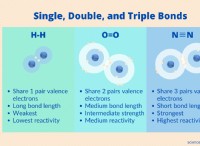
* Διαμοριακές δυνάμεις: Τα ιόντα άλατος (Na+ και Cl-) αλληλεπιδρούν με μόρια νερού μέσω ηλεκτροστατικών δυνάμεων, διαταράσσοντας τους δεσμούς υδρογόνου μεταξύ των μορίων νερού. Αυτό καθιστά πιο δύσκολο για τα μόρια του νερού να ξεφύγουν στη φάση ατμών.
* Πίεση ατμών: Η πίεση ατμών του διαλύματος είναι χαμηλότερη από αυτή του καθαρού νερού στην ίδια θερμοκρασία. Αυτό σημαίνει ότι απαιτείται περισσότερη ενέργεια (και επομένως υψηλότερη θερμοκρασία) για να φτάσουμε στο σημείο όπου η πίεση του ατμού ισούται με την ατμοσφαιρική πίεση και τη βρασμό.
* Colligative Property: Η ανύψωση του σημείου βρασμού είναι μια περιφερειακή ιδιότητα, που σημαίνει ότι εξαρτάται από τον αριθμό των σωματιδίων διαλυμένης ουσίας που διαλύονται, όχι από τον συγκεκριμένο τύπο διαλυμένης ουσίας. Όσο περισσότερα σωματίδια διαλύονται, τόσο μεγαλύτερη είναι η αύξηση του σημείου βρασμού.
Εν ολίγοις, η προσθήκη αλατιού στο νερό καθιστά πιο δύσκολο το νερό να βράσει, οπότε το σημείο βρασμού ανεβαίνει.