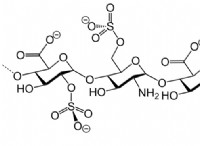
Τι είναι ψευδές σχετικά με τους χημικούς δεσμούς;
* Οι δεσμοί είναι πάντα "σπασμένοι" σε χημικές αντιδράσεις. Ενώ πολλές αντιδράσεις περιλαμβάνουν το σπάσιμο των δεσμών, ορισμένες αντιδράσεις περιλαμβάνουν σχηματισμό δεσμών και άλλες περιλαμβάνουν τόσο το σπάσιμο όσο και τη διαμόρφωση νέων δεσμών.
* Όλοι οι δεσμοί είναι εξίσου ισχυροί. Τα ομόλογα ποικίλλουν σε μεγάλο βαθμό σε δύναμη. Οι ιοντικοί δεσμοί είναι γενικά ισχυρότεροι από τους ομοιοπολικούς δεσμούς και οι διάφοροι τύποι ομοιοπολικών δεσμών έχουν διαφορετικά πλεονεκτήματα (π.χ., οι διπλοί δεσμοί είναι ισχυρότεροι από τους μεμονωμένους δεσμούς).
* Οι χημικοί δεσμοί είναι άκαμπτοι και αμετάβλητοι. Ενώ τα ομόλογα έχουν συγκεκριμένο χαρακτήρα, δεν είναι στατικοί. Τα μήκη και τα πλεονεκτήματα των δεσμών μπορούν να αλλάξουν λόγω παραγόντων όπως η θερμοκρασία, η πίεση και η παρουσία άλλων μορίων.
* Οι δεσμοί εμφανίζονται μόνο μεταξύ δύο ατόμων Ενώ πολλοί κοινοί δεσμοί είναι μεταξύ δύο ατόμων, υπάρχουν επίσης πολλαπλοί δεσμοί, όπου περισσότερα από δύο άτομα μοιράζονται ηλεκτρόνια.
* Οι χημικοί δεσμοί είναι τα μόνα μόρια που συγκρατούν τη δύναμη. Ενώ οι δεσμοί είναι η πρωταρχική δύναμη, άλλες δυνάμεις, όπως οι δυνάμεις van der Waals και η δέσμευση υδρογόνου, παίζουν επίσης ρόλο στη συγκράτηση των μορίων μαζί.
* Όλοι οι δεσμοί σχηματίζονται με κοινή χρήση ηλεκτρονίων. Οι ιοντικοί δεσμοί σχηματίζονται με τη μεταφορά ηλεκτρονίων, που δεν μοιράζονται.
Σημαντική σημείωση: Το πλαίσιο της ερώτησης είναι ζωτικής σημασίας για τον προσδιορισμό του τι είναι "ψευδές" για τους χημικούς δεσμούς. Οι παραπάνω δηλώσεις είναι γενικές παρανοήσεις, αλλά ανάλογα με το συγκεκριμένο πλαίσιο, άλλες πτυχές της χημικής σύνδεσης θα μπορούσαν να θεωρηθούν ψευδείς.