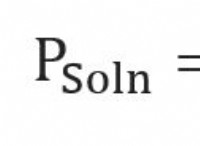Είναι αλήθεια ότι τα σωματίδια διαλύματος δεν αναμειγνύονται στο ατομικό ή μοριακό επίπεδο;
διαλύματα σχηματίζονται όταν τα σωματίδια αναμειγνύονται στο ατομικό ή μοριακό επίπεδο. Εδώ είναι γιατί:
* Λύσεις είναι ομοιογενή μείγματα. Αυτό σημαίνει ότι τα συστατικά κατανέμονται ομοιόμορφα σε όλο το μείγμα, πράγμα που σημαίνει ότι αναμιγνύονται στο μικρότερο δυνατό επίπεδο.
* διαλυμένα (οι ουσίες που διαλύονται) χωρίζονται σε μεμονωμένα μόρια ή ιόντα και στη συνέχεια περιβάλλονται από διαλύτη (Η ουσία που κάνει τη διάλυση) Μόρια. Αυτή η αλληλεπίδραση ονομάζεται διαλυτοποίηση .
* Παράδειγμα: Όταν διαλύετε το άλας (NaCl) στο νερό (H₂O), οι κρύσταλλοι αλατιού διασπώνται σε ιόντα Na⁺ και CL⁻, τα οποία στη συνέχεια περιβάλλονται από μόρια νερού. Το αποτέλεσμα είναι ένα ομοιογενές διάλυμα αλατιού που διαλύεται σε νερό.
Είναι σημαντικό να σημειωθεί ότι:
* Η έκταση της ανάμειξης στο ατομικό/μοριακό επίπεδο μπορεί να ποικίλει ανάλογα με τον τύπο του διαλύματος (π.χ. ισχυρή έναντι ασθενούς ηλεκτρολύτη).
* Οι λύσεις είναι διαφορετικές από το εναιωρήματα , όπου τα σωματίδια είναι μεγαλύτερα και δεν αναμειγνύονται στο ατομικό/μοριακό επίπεδο.
Επιτρέψτε μου να ξέρω αν έχετε άλλες ερωτήσεις!