Τι επίδραση έχει η περιστροφή ενός ηλεκτρονίου σε μακροεπίπεδα;
Η περιστροφή ηλεκτρονίων συμβάλλει στο φαινόμενο Zeeman, το οποίο χρησιμοποιείται για τη μελέτη των μαγνητικών πεδίων στον διαστρικό χώρο και την πρόβλεψη του σχηματισμού άστρων.
Όταν ακούτε τη λέξη ηλεκτρόνιο , αυτό που έρχεται στο μυαλό είναι πιθανώς μια εξαιρετικά μικρή, αρνητικά φορτισμένη σφαίρα, η ηλεκτρονική διαμόρφωση των στοιχείων και πιθανώς το γεγονός ότι το ηλεκτρικό ρεύμα οφείλεται στη ροή των ηλεκτρονίων σε ένα σύρμα. Ωστόσο, όντας φορτισμένα και σε κίνηση, έχουν επίσης μαγνητικές ιδιότητες, οι οποίες προκαλούν αρκετά ενδιαφέροντα φαινόμενα σε κβαντική κλίμακα, που έχουν συνέπειες ακόμη και στη διαστρική κλίμακα.
Η εγγενής ιδιότητα των ηλεκτρονίων που συμβάλλει στον μαγνητισμό ονομάζεται spin . Για να κατανοήσετε τα αποτελέσματα της περιστροφής σε μακροοικονομική κλίμακα, είναι σημαντικό πρώτα να κατανοήσετε τι είναι η περιστροφή.
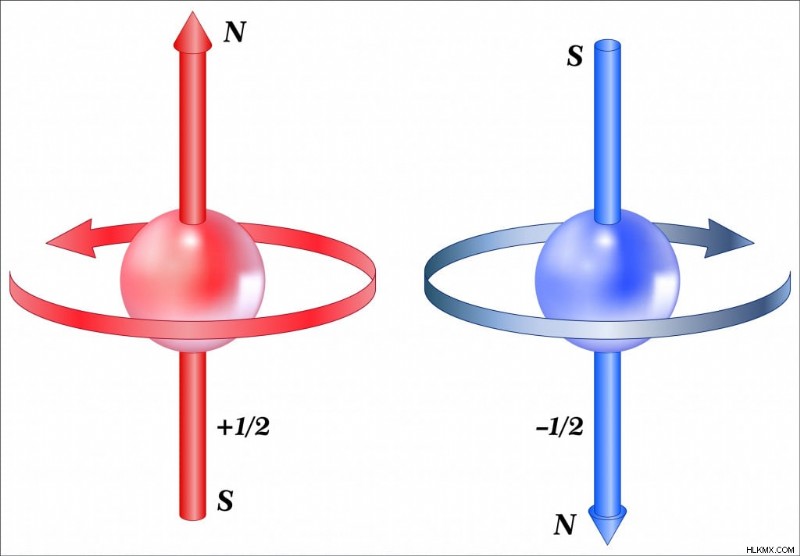
Ένα ηλεκτρόνιο συμπεριφέρεται σαν να ήταν μια περιστρεφόμενη σφαίρα, η οποία έχει ως αποτέλεσμα την παραγωγή μαγνητικών πεδίων. (Φωτογραφία :Fouad A. Saad/Shutterstock)
Electron Spin:A Misnomer
Η θεωρία του Bohr για το άτομο ήταν μια επέκταση της κλασικής θεωρίας στον κβαντικό κόσμο. Στην ουσία, τα ηλεκτρόνια υποτίθεται ότι περιφέρονται γύρω από τον πυρήνα, όπως ακριβώς η Γη περιφέρεται γύρω από τον ήλιο. Έτσι, ολόκληρο το μαθηματικό πλαίσιο του συστήματος ήλιου-γης (υπολογισμός γωνιακής ορμής, γωνιακής ταχύτητας, ενέργειας περιστροφής και περιστροφής κ.λπ.) επεκτάθηκε στο σύστημα ηλεκτρονίου-πυρήνα.
Δεδομένου ότι ένα ηλεκτρόνιο συμπεριφέρεται ως σημειακό φορτίο χωρίς χωρική κατανομή μάζας , η περιστρεφόμενη αναλογία της κλασικής μηχανικής απορρίφθηκε και διατηρήθηκε μόνο η τροχιακή αναλογία (δηλαδή η επανάσταση γύρω από τον πυρήνα). Έτσι, ένα ηλεκτρόνιο υποτέθηκε ότι έχει τροχιακή γωνιακή ορμή και μια σχετική τροχιακή μαγνητική ροπή .
Αργότερα πειράματα έδειξαν ότι τα ηλεκτρόνια έχουν μια εγγενή μαγνητική ροπή και μια εγγενή γωνιακή ορμή, οι οποίες είναι ανεξάρτητες από την τροχιακή συνιστώσα.
Αυτό βαφτίστηκε στροφική γωνιακή ορμή και μαγνητική ροπή περιστροφής γιατί είχε νόημα όταν σκεφτόταν από την κλασική προοπτική. Τα ηλεκτρόνια δεν περιστρέφονται επειδή θα παραβίαζε τους νόμους της ειδικής σχετικότητας . Επομένως, το Spin είναι μια εσφαλμένη ονομασία και δεν πρέπει να συγχέεται με τη φυσική περιστροφή αντικειμένων.
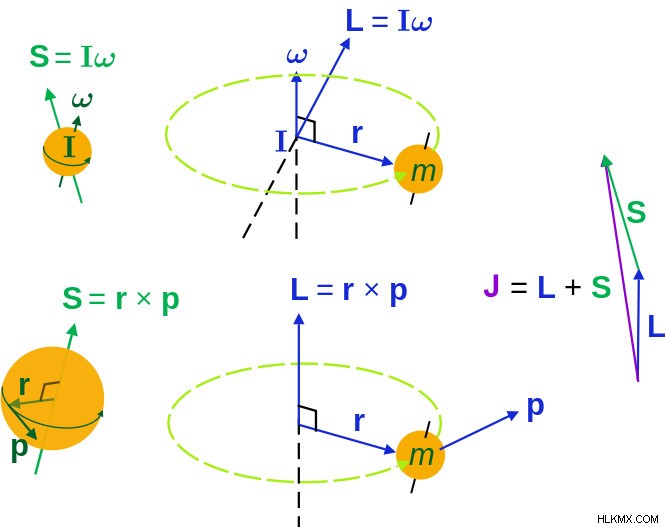
Το L είναι η τροχιακή γωνιακή ορμή και το S είναι η γωνιακή ορμή σπιν. Το J είναι η συνολική γωνιακή ορμή, η οποία είναι το διανυσματικό άθροισμα των L και S. (Προστασία φωτογραφίας :Maschen/Wikimedia commons)
Εφέ της περιστροφής ηλεκτρονίων:The Zeeman Effect
Θεωρήστε ένα άτομο υδρογόνου. Ο Bohr υπέθεσε ότι υπάρχουν μόνο συγκεκριμένες τροχιές που μπορεί να πάρει ένα ηλεκτρόνιο. Αυτές ονομάζονταν στάσιμες καταστάσεις . Ένας βολικός τρόπος αναπαράστασης αυτών ήταν χρησιμοποιώντας τον κύριο κβαντικό αριθμό n, όπου n αντιπροσώπευε τον αριθμό τροχιάς. Για παράδειγμα, n=1 ήταν η χαμηλότερη τροχιά (πλησιέστερα στον πυρήνα και η πιο σταθερή), n=2 ήταν η επόμενη επιτρεπόμενη τροχιά με ενέργεια μεγαλύτερη από n=1 . Ομοίως, περαιτέρω τροχιές ορίστηκαν ως n=3, 4, 5, …, κλπ. Όσο μεγαλύτερη είναι η τιμή του n , τόσο μεγαλύτερη είναι η ενέργεια του ηλεκτρονίου.
Το nth η τροχιά δίνεται από:
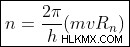 , όπου
, όπου
h =Η σταθερά του Planck,
m =Μάζα του ηλεκτρονίου,
v =Γραμμική ταχύτητα της τροχιακής κίνησης του ηλεκτρονίου,
R =ακτίνα της νης τροχιάς
Η παροχή ενέργειας στα ηλεκτρόνια τα προωθεί σε καταστάσεις υψηλότερης ενέργειας (από n=1 σε n=2, 3, 4 , …, και τα λοιπά.). Όταν τα ενεργειακά διεγερμένα ηλεκτρόνια πέφτουν πίσω στη θεμελιώδη κατάσταση, εκπέμπουν ηλεκτρομαγνητική ακτινοβολία με ενέργεια ίση με τη διαφορά ενέργειας των δύο κύριων κβαντικών καταστάσεων. Αυτές οι μεταβάσεις μπορούν να προβληθούν μέσω ενός φασματόμετρου , και το φάσμα ονομάζεται φάσμα εκπομπής .

Φάσμα εκπομπής ατόμου υδρογόνου. Μια κλίμακα κάτω από το φάσμα μετρά τη θέση εμφάνισης, η οποία υποδεικνύει το μήκος κύματος της μετάβασης. (Φωτογραφία:Patrick Edwin Mora/Wikimedia commons)
Όταν το φάσμα εκπομπής του υδρογόνου αναλύεται παρουσία εξωτερικού μαγνητικού πεδίου, εμφανίζεται ένα περίεργο φαινόμενο. Η θεωρία του Bohr προέβλεψε σωστά τη διάσπαση των γραμμών σε τρίδυμα για το n=3 σε n=2 μετάβαση, λαμβάνοντας υπόψη μόνο την τροχιακή γωνιακή ορμή . Ωστόσο, όταν αναλύεται το φάσμα του νατρίου, οι γραμμές που αντιστοιχούν σε διάφορες μεταβάσεις, όπως n=3 σε n=2 ή n=4 έως n=3 χωρίστηκε σε περισσότερες από τρεις γραμμές, κάτι που όχι προβλέπεται από τη θεωρία του Bohr.
Θα μπορούσε να εξηγηθεί μόνο από την ύπαρξη μιας εγγενούς μαγνητικής ροπής, που ονομάζεται μαγνητική ροπή περιστροφής . Αυτή η μαγνητική ροπή σπιν αλληλεπιδρά με την τροχιακή μαγνητική ροπή για να δημιουργήσετε τις πολλαπλές γραμμές σε κοντινή απόσταση.
Μαθηματικά, οι τροχιακές και οι μαγνητικές ροπές σπιν δίνονται από:
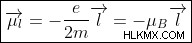 και
και 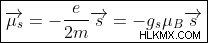 αντίστοιχα, όπου,
αντίστοιχα, όπου,
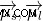 =Μαγνητική ροπή περιστροφής και τροχιακή μαγνητική ροπή, αντίστοιχα,
=Μαγνητική ροπή περιστροφής και τροχιακή μαγνητική ροπή, αντίστοιχα,
e =φορτίο στο ηλεκτρόνιο
μ =μάζα του ηλεκτρονίου.
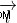 ,
, 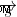 =Τροχιακή γωνιακή ορμή και γωνιακή ορμή περιστροφής, αντίστοιχα,
=Τροχιακή γωνιακή ορμή και γωνιακή ορμή περιστροφής, αντίστοιχα,
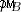 =Bohr Magneton,
=Bohr Magneton,
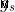 =Ο συντελεστής g spin του Lande ~ 2.002
=Ο συντελεστής g spin του Lande ~ 2.002
Όταν αυτά τα δύο αθροίζονται, η προκύπτουσα μαγνητική ροπή δίνεται από το
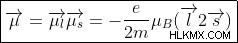
Αυτή η μαγνητική ροπή είναι υπεύθυνη για το Φαινόμενο Zeeman . Η διάσπαση των γραμμών παρουσία ενός εξωτερικού μαγνητικού πεδίου υποδηλώνει ότι συμβαίνει επίσης μια αλλαγή συχνότητας. Η μετατόπιση συχνότητας δίνεται από:
 όπου
όπου
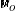 =μη μετατοπισμένη συχνότητα
=μη μετατοπισμένη συχνότητα
g =ο συντελεστής g του Lande
B =Ένταση μαγνητικού πεδίου
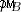 =Bohr Magneton
=Bohr Magneton
h =Η σταθερά του Planck
Από την παραπάνω εξίσωση, B μπορεί να υπολογιστεί εάν η συχνότητα είναι γνωστή. Αυτή η συχνότητα μετριέται χρησιμοποιώντας ένα φασματόμετρο.
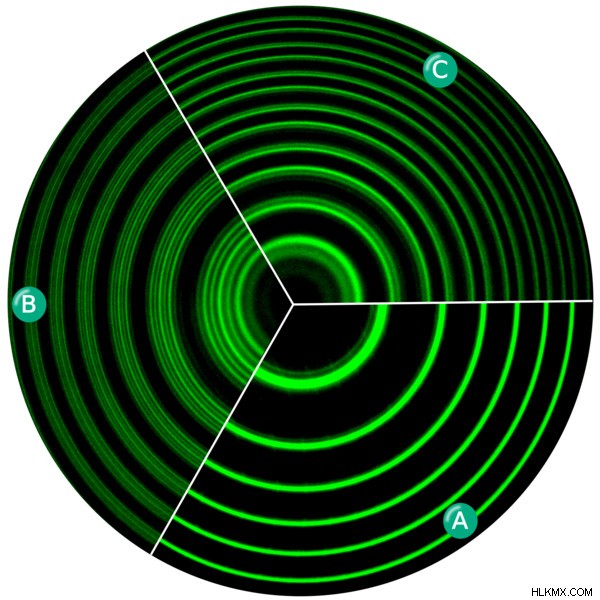
Φασματικές γραμμές ατμού υδραργύρου. Το Α είναι χωρίς μαγνητικό πεδίο. Το B είναι με ένα μαγνητικό πεδίο που παράγει ένα εγκάρσιο φαινόμενο Zeeman και το C δείχνει το διαμήκη φαινόμενο Zeeman. (Φωτογραφία:Warren Leywon/Wikimedia Commons)
Εφέ του Spin στη Μακρο Κλίμακα
Είδαμε ότι η μαγνητική ροπή σπιν αλληλεπιδρά με την τροχιακή μαγνητική ροπή και το εξωτερικό μαγνητικό πεδίο, έτσι ώστε τα επίπεδα ενέργειας να χωρίζονται. Σε μακροοικονομική κλίμακα, αυτό χρησιμοποιείται στην αστροφυσική.
Μελέτη Σχηματισμού Αστέρων στο Διαστρικό Διάστημα
Ο διαστρικός χώρος αποτελείται από διάφορα αέρια, όπως H2, CO, OH, HI κ.λπ., με το πιο άφθονο αέριο Υδρογόνο. Αυτά τα αέρια, μαζί με τα πολύ λεπτά σωματίδια σκόνης, δημιουργούν ένα σύννεφο αερίων. Δεδομένου ότι η βαρύτητα είναι μια εγγενής ιδιότητα της μάζας, αυτά τα αέρια συγκεντρώνονται για να σχηματίσουν μεγάλα νέφη αερίων, τα οποία αυξάνουν την πυκνότητα μάζας σε αυτήν την περιοχή του διαστήματος, με αποτέλεσμα μεγαλύτερη βαρυτική δύναμη, η οποία συσσωρεύει ακόμη περισσότερη ύλη. Έτσι, δημιουργείται ένας βρόχος θετικής ανάδρασης όπου η βαρύτητα συμπιέζει τη μάζα μαζί, με αποτέλεσμα την αύξηση της βαρυτικής έλξης λόγω της συμπιεσμένης μάζας.
Ο διαστρικός χώρος περιέχει επίσης ασθενή μαγνητικά πεδία της τάξης ~ 3uG – 6uG. Σε συνθήκες ισορροπίας, αυτό το μαγνητικό πεδίο εξισορροπεί τη βαρυτική έλξη των νεφών αερίου και εμποδίζει την περαιτέρω συσσώρευση μάζας. Ο λόγος της μαγνητικής ροής προς τη μάζα του νέφους είναι χρήσιμος για τη μελέτη του σχηματισμού άστρων.
Θεωρητικές προβλέψεις
Υποθέτοντας μια σφαιρική μάζα διαστρικού νέφους, ο λόγος ισορροπίας της μαγνητικής ροής (ποσότητα του μαγνητικού πεδίου που υπάρχει σε αυτήν την περιοχή) προς τη μάζα του νέφους, που ονομάζεται κρίσιμος λόγος μάζας προς ροή δίνεται από:
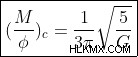 όπου,
όπου,
M =Μάζα του νέφους αερίου
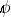 =Μαγνητική ροή
=Μαγνητική ροή
G =Καθολική Σταθερά Βαρύτητας ~ 6,674  10-11 m3/kg/s2
10-11 m3/kg/s2
Αυτή είναι η θεωρητική κριτική αναλογία βασίζεται σε υπολογισμούς όπου η βαρυτική έλξη εξισορροπείται από μαγνητικές δυνάμεις.
Φασματικές Παρατηρήσεις
Το φάσμα εκπομπής από αυτήν την περιοχή του διαστήματος αναλύεται και η πραγματική ισχύς του μαγνητικού πεδίου B υπολογίζεται χρησιμοποιώντας την ακόλουθη εξίσωση:
 , από την οποία η ροή, Υπολογίζεται το
, από την οποία η ροή, Υπολογίζεται το 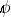 .
.
Παρατηρείται η μάζα του νέφους αερίου (αυτή η διαδικασία ξεφεύγει από το πεδίο εφαρμογής αυτού του άρθρου) και η παρατηρούμενη ( 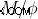 ) Υπολογίζεται ο λόγος.
) Υπολογίζεται ο λόγος.
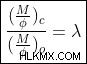

Ο σχηματισμός άστρων στο διαστρικό διάστημα υπαγορεύεται από την αλληλεπίδραση μεταξύ των μαγνητικών πεδίων και της βαρυτικής έλξης. (Φωτογραφία :Antares_StarExplorer/Shutterstock)
Περίπτωση Ι :Αν 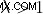 , τότε η μάζα του νέφους είναι υπερκρίσιμη και το μαγνητικό πεδίο δεν είναι σε θέση να σταματήσει τη βαρυτική κατάρρευση της μάζας στον εαυτό του, με αποτέλεσμα τον πιθανό σχηματισμό αστεριών.
, τότε η μάζα του νέφους είναι υπερκρίσιμη και το μαγνητικό πεδίο δεν είναι σε θέση να σταματήσει τη βαρυτική κατάρρευση της μάζας στον εαυτό του, με αποτέλεσμα τον πιθανό σχηματισμό αστεριών.
Υπόθεση II :Αν 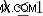 , τότε το μαγνητικό πεδίο από μόνο του είναι αρκετό για να σταματήσει τα νέφη αερίου από τη βαρυτική κατάρρευση.
, τότε το μαγνητικό πεδίο από μόνο του είναι αρκετό για να σταματήσει τα νέφη αερίου από τη βαρυτική κατάρρευση.
Μια τελευταία λέξη
Τα ηλεκτρόνια έχουν δύο μαγνητικές ροπές που συνδέονται με αυτά, μια τροχιακή μαγνητική ροπή και μια μαγνητική ροπή σπιν. Η αλληλεπίδραση αυτών των στιγμών προκαλεί τη διάσπαση των ενεργειακών επιπέδων παρουσία ενός εξωτερικού μαγνητικού πεδίου, ένα φαινόμενο που ονομάζεται Φαινόμενο Zeeman.
Ο διαστρικός χώρος περιέχει επίσης ασθενή μαγνητικά πεδία. Όταν παρατηρείται μια περιοχή ενδιαφέροντος, το φάσμα εκπομπών περιέχει επίσης λεπτές γραμμές, που αντιστοιχούν στα διαχωρισμένα επίπεδα ενέργειας. Στη συνέχεια χρησιμοποιείται για τον υπολογισμό του μαγνητικού πεδίου σε μια δεδομένη περιοχή του χώρου.
Με αυτόν τον τρόπο, ένα κβαντικό φαινόμενο μπορεί να χρησιμοποιηθεί για την παρατήρηση επιδράσεων μακρο-κλίμακας!




