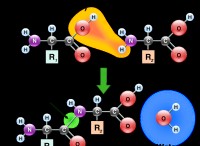
Οξείδωση και Αναγωγή
Όταν αλλάζουν οι καταστάσεις οξείδωσης των ατόμων, μια χημική διεργασία λέγεται οξειδοαναγωγή και ορίζεται ως εξής:Χαρακτηρίζεται από την πραγματική ή τυπική μεταφορά ηλεκτρονίων μεταξύ χημικών ειδών, με την πλειοψηφία των αντιδράσεων οξειδοαναγωγής που περιλαμβάνουν ένα είδος (ο αναγωγικός παράγοντας) που περνάει από οξείδωση (και επομένως χάνει ηλεκτρόνια) ενώ ένα άλλο είδος (ο οξειδωτικός παράγοντας) περνά από αναγωγή (και έτσι αποκτά ηλεκτρόνια) (κερδίζει ηλεκτρόνια). Αυτή η διαδικασία αναφέρεται ως οξείδωση για τα χημικά είδη από τα οποία αποσύρεται το ηλεκτρόνιο και αναγωγή για τα χημικά είδη στα οποία έχει εισαχθεί το ηλεκτρόνιο. Για να το θέσω αλλιώς:
Η οξείδωση ορίζεται ως η απώλεια ηλεκτρονίων ή η αύξηση της κατάστασης οξείδωσης ενός ατόμου, ενός ιόντος ή συγκεκριμένων ατόμων σε ένα μόριο ως αποτέλεσμα της παρουσία οξυγόνου στο σύστημα.
Ένα άτομο, ένα ιόν ή ένα συγκεκριμένο άτομο ή υποατομικό σωματίδιο υφίσταται αναγωγή όταν αποκτά ηλεκτρόνια και/ή μειώνει την κατάσταση οξείδωσης του ατόμου, του ιόντος ή το συγκεκριμένο άτομο ή υποατομικό σωματίδιο (μείωση στην κατάσταση οξείδωσης).
Πολλές αντιδράσεις στην οργανική χημεία είναι αντιδράσεις οξειδοαναγωγής, οι οποίες συμβαίνουν ως αποτέλεσμα αλλαγών στις καταστάσεις οξείδωσης, αλλά δεν περιλαμβάνουν ξεχωριστή μεταφορά ηλεκτρονίων. Αυτές οι αντιδράσεις περιλαμβάνουν:Για παράδειγμα, όταν το ξύλο καίγεται με μοριακό οξυγόνο, η κατάσταση οξείδωσης των ατόμων άνθρακα στο ξύλο αυξάνεται ενώ η κατάσταση οξείδωσης των ατόμων οξυγόνου πέφτει, με αποτέλεσμα το σχηματισμό διοξειδίου του άνθρακα και νερού. Τα άτομα οξυγόνου περνούν από μια διαδικασία αναγωγής, κερδίζοντας τυπικά ηλεκτρόνια, ενώ τα άτομα άνθρακα περνούν από μια διαδικασία οξείδωσης, χάνοντας επίσημα ηλεκτρόνια. Ως αποτέλεσμα, το οξυγόνο χρησιμεύει ως οξειδωτικός παράγοντας σε αυτή τη διαδικασία, ενώ ο άνθρακας ως αναγωγικός παράγοντας.
Ωστόσο, παρόλο που οι αντιδράσεις οξείδωσης συνδέονται γενικά με τη δημιουργία οξειδίων από μόρια οξυγόνου, δεν απαιτείται πάντα να υπάρχει οξυγόνο σε τέτοιες αντιδράσεις, επειδή άλλα χημικά είδη μπορούν να έχουν τον ίδιο ρόλο με το οξυγόνο.
Οξείδωση
Οι παραδοσιακές ή προηγούμενες έννοιες της οξείδωσης ορίζουν τη διαδικασία ως εκείνη κατά την οποία προστίθεται οξυγόνο ή οποιοδήποτε ηλεκτραρνητικό στοιχείο, ενώ λαμβάνει χώρα η αφαίρεση υδρογόνου ή οποιουδήποτε ηλεκτροθετικού στοιχείου.
Στην ηλεκτρονική θεωρία, η οξείδωση ορίζεται ως η διαδικασία κατά την οποία ένα άτομο ή ιόν χάνει ένα ή περισσότερα ηλεκτρόνια ως αποτέλεσμα μιας χημικής αντίδρασης.
Μείωση
Η αναγωγή, σύμφωνα με την κλασική ή παλαιότερη έννοια, είναι μια διαδικασία που περιλαμβάνει την προσθήκη υδρογόνου ή οποιουδήποτε ηλεκτροθετικού στοιχείου, καθώς και την αφαίρεση οξυγόνου ή οποιουδήποτε ηλεκτραρνητικού στοιχείου.
Η αναγωγή, σύμφωνα με την ηλεκτρονική έννοια, περιγράφεται ως η διαδικασία με την οποία ένα άτομο ή ένα ιόν λαμβάνει ένα ή περισσότερα ηλεκτρόνια από ένα άλλο
Η κλασική έννοια των αντιδράσεων οξείδωσης και αναγωγής είναι η εξής:
Τα παρακάτω είναι παραδείγματα αντιδράσεων οξείδωσης:
1. Προσθήκη οξυγόνου:
C + O2 → CO2 (οξείδωση του άνθρακα)
2. Προσθήκη ηλεκτραρνητικού στοιχείου:
Fe + S → FeS (οξείδωση του σιδήρου)
3. Αφαίρεση υδρογόνου από το σύστημα:
H2S + Br2 → 2 HBr + S (οξείδωση του σουλφιδίου)
4. Αφαίρεση ηλεκτροθετικών στοιχείων:
2 KI + H2O2 → I2 + 2 KOH (οξείδωση ιωδίου)
Ένας οξειδωτικός παράγοντας είναι μια χημική ουσία που προκαλεί την οξείδωση. Μεταξύ των οξειδωτικών παραγόντων που χρησιμοποιούνται στις παραπάνω περιπτώσεις είναι το οξυγόνο, το διοξείδιο του θείου, το διοξείδιο του χλωρίου, το διοξείδιο του βρωμίου και το υπεροξείδιο του υδρογόνου.
Οι αντιδράσεις μείωσης περιλαμβάνουν τα ακόλουθα βήματα:
1. Προσθήκη υδρογόνου
N2 + 3 H2 → 2NH3 (μείωση αζώτου)
2. Προσθήκη ηλεκτροθετικού στοιχείου:
SnCl2 + 2HgCl2 → SnCl4 + Hg2Cl2 (μείωση χλωριούχου υδραργύρου)
3. Αφαίρεση οξυγόνου
ZnO + C → Zn + CO (μείωση του οξειδίου του ψευδαργύρου)
4. Αφαίρεση ηλεκτραρνητικού στοιχείου
2FeCl3 + H2 → 2FeCl2 + 2HCl (μείωση χλωριούχου σιδήρου)
Ένας αναγωγικός παράγοντας είναι μια χημική ουσία που έχει ως αποτέλεσμα τη μείωση της ποσότητας κάτι. Στις παραπάνω περιπτώσεις, χρησιμοποιούνται οι αναγωγικοί παράγοντες H2, HgCl2 και C.
Οξείδωση και αναγωγή ως προς τη μεταφορά ηλεκτρονίων
Σαν γενικό κανόνα, αυτός είναι ο πιο γενικά χρησιμοποιούμενος και πιο εκτενώς εφαρμόσιμος ορισμός της οξείδωσης και της αναγωγής.
Σε αυτήν την περίπτωση, η οξείδωση ορίζεται ως η απώλεια ηλεκτρονίων και η αναγωγή ορίζεται ως η απόκτηση ηλεκτρονίων.
Η εξέδρα άντλησης πετρελαίου είναι ένα ιδιαίτερα αποτελεσματικό μνημονικό για να θυμάστε αυτό το θέμα.
OIL RIG, Οξείδωση είναι η απώλεια μιας ουσίας. Το κέρδος προέρχεται από τη μείωση.
Οι αντιδράσεις οξείδωσης και αναγωγής είναι άρρηκτα συνυφασμένες στη φύση. Για το λόγο ότι τα ηλεκτρόνια ούτε παράγονται ούτε καταστρέφονται σε μια χημική διεργασία, οι αντιδράσεις οξείδωσης και αναγωγής συμβαίνουν πάντα σε ζεύγη. είναι, επομένως, αδύνατο να υπάρχει το ένα χωρίς το άλλο. Χρησιμοποιώντας την ακόλουθη διαδικασία ως παράδειγμα, το μαγνήσιο οξειδώνεται δίνοντας δύο ηλεκτρόνια στο οξυγόνο, το οποίο στη συνέχεια ανάγεται απορροφώντας δύο ηλεκτρόνια από το μαγνήσιο.
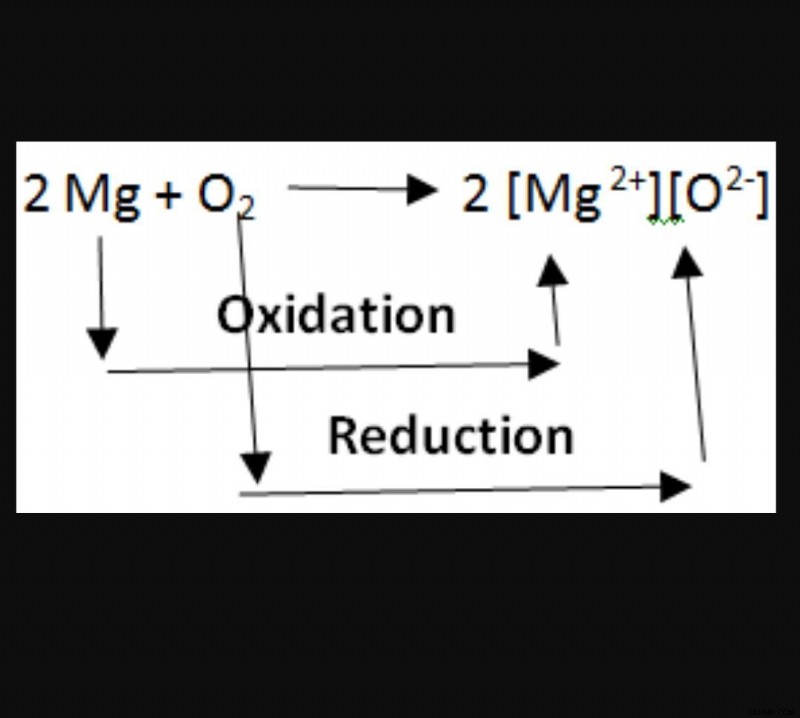
Επειδή η οξείδωση και η αναγωγή δεν μπορούν να συμβούν μεμονωμένα, αναφέρονται ως "αντιδράσεις οξειδοαναγωγής" όταν εμφανίζονται ως ομάδα. Το αντιδραστήριο που οξειδώνει τα άλλα αντιδρώντα αναφέρεται ως οξειδωτικός παράγοντας, ενώ το αντιδραστήριο που ανάγει τα άλλα αντιδραστήρια αναφέρεται ως αναγωγικός παράγοντας. Υπάρχει μεγάλη ασάφεια σχετικά με το εάν οι οξειδωτικοί παράγοντες λαμβάνουν ή εκχωρούν ηλεκτρόνια.
Συνήθεις αντιδράσεις οξειδοαναγωγής
Οι παρακάτω είναι οι τρεις πιο διαδεδομένες αντιδράσεις οξειδοαναγωγής που συμβαίνουν:
1. Αντίδραση καύσης — Πρόκειται για ένα είδος οξειδοαναγωγικής αντίδρασης που συμβαίνει μεταξύ μοριακού οξυγόνου και μιας χημικής ουσίας, με αποτέλεσμα τον σχηματισμό προϊόντων που περιλαμβάνουν οξυγόνο.
2C8H18+25O2 → 16CO2(g)+18H2O
2.Είναι μια αντίδραση οξειδοαναγωγής στην οποία μόνο ένα αντιδρών ανάγεται και στη συνέχεια οξειδώνεται, η οποία είναι γνωστή ως αντίδραση δυσαναλογίας. Μια αντίδραση αυτοοξείδωσης είναι ένας άλλος όρος για αυτό το φαινόμενο.
3ClO−(aq) → ClO3−(aq)+2Cl−(aq)
3. Οι αντιδράσεις απλής αντικατάστασης (γνωστές και ως αντιδράσεις απλής υποκατάστασης) είναι ένας τύπος αντίδρασης οξειδοαναγωγής κατά την οποία δύο στοιχεία μεταφέρουν θέσεις μέσα σε ένα μόριο. Μια απλή αντίδραση μετατόπισης είναι ένα άλλο όνομα για αυτόν τον τύπο αντίδρασης.
Zn(s)+2HCl(aq) → ZnCl2(aq)+H2(g)
Συμπέρασμα
Οι όροι οξείδωση και αναγωγή μπορούν να οριστούν ως η προσθήκη ή αφαίρεση οξυγόνου από μια ουσία, αντίστοιχα. Αν και αυτός δεν είναι ο πιο ολοκληρωμένος ορισμός, όπως θα περιγραφεί παρακάτω, είναι ο πιο εύκολα απομνημονευμένος. Η οξείδωση είναι η διαδικασία πρόσληψης οξυγόνου. Η απώλεια οξυγόνου αναφέρεται ως μείωση. Οι αντιδράσεις οξείδωσης-αναγωγής (γνωστές και ως αντιδράσεις οξειδοαναγωγής) είναι απαραίτητες επειδή είναι οι πρωταρχικές πηγές ενέργειας σε αυτόν τον πλανήτη, είτε υπάρχουν φυσικά είτε βιολογικά παράγονται και παράγονται τεχνητά. Η οξείδωση των μορίων, είτε με την αφαίρεση υδρογόνου είτε με συνδυασμό με οξυγόνο, συνήθως οδηγεί στην απελευθέρωση τεράστιων ποσοτήτων ενέργειας.