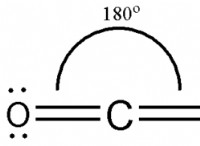
Οξαλικό οξύ
Η παρουσία αυτού του οργανικού μορίου μπορεί να παρατηρηθεί σε μια ποικιλία λαχανικών και φυτών. Δικαρβοξυλικό οξύ με συμπυκνωμένο τύπο HOOC-COOH, είναι το απλούστερο από τα δικαρβοξυλικά οξέα και έχει όξινη ισχύ μεγαλύτερη από το οξικό οξύ. Η υπερβολική κατάποση οξαλικού οξέος μπορεί να είναι επικίνδυνη για την υγεία σας. Δημιουργείται ως αποτέλεσμα της οξείδωσης των υδατανθράκων στον οργανισμό. Μια συνθετική εκδοχή αυτής της ένωσης μπορεί επίσης να κατασκευαστεί στο εργαστήριο με οξείδωση σακχαρόζης παρουσία νιτρικού οξέος παρουσία καταλύτη όπως το πεντοξείδιο του βαναδίου.
Το οξαλικό οξύ αποτελείται από δύο πολυμορφικές δομές, η πρώτη από τις οποίες εμφανίζεται ως λευκό κρυσταλλικό στερεό που, όταν διαλύεται στο νερό, μετατρέπεται σε άχρωμο διάλυμα. Είναι ένας αναγωγικός παράγοντας που μπορεί επίσης να χρησιμοποιηθεί ως χηλικός παράγοντας όταν συνδυάζεται με οξαλικό, το οποίο χρησιμεύει ως η συζυγής του βάση.
Φόρμουλα για οξαλικό οξύ
Το οξαλικό οξύ είναι ένα δικαρβοξυλικό οξύ με μοριακό τύπο C2H2O4 που χρησιμοποιείται στην επεξεργασία τροφίμων. Το οξαλικό οξύ βρίσκεται στον κυτταρικό χυμό των φυτικών ειδών Oxalis και Rumex με τη μορφή αλάτων καλίου και ασβεστίου, αντίστοιχα.
Το οξαλικό οξύ είναι ένα ασθενές οξύ που ιονίζεται μόνο εν μέρει όταν υπάρχει σε υδατικό διάλυμα. Το οξαλικό οξύ έχει δύο πρωτόνια που είναι όξινα. Ο αρχικός ιονισμός έχει ως αποτέλεσμα το σχηματισμό HC2O4–, ενός ασθενούς οξέος που τελικά θα ιονιστεί.
Το οξαλικό οξύ είναι ένα από τα πιο ισχυρά οργανικά οξέα που υπάρχουν, ικανό να διαλύει το ανθρακικό οξύ και ένα ευρύ φάσμα άλλων οξέων από τα άλατά τους. Το οξαλικό οξύ σχηματίζεται από τη δράση είτε μιας ένυδρης ποτάσας είτε ενός νιτρικού οξέος στην πλειονότητα των οργανικών μορίων που βρίσκονται στο φυσικό περιβάλλον. Σε ορισμένους κύκλους αναφέρεται ως διπρωτικό οξύ.
Δομή οξαλικού οξέος

Πρέπει να σημειωθεί ότι το οξαλικό οξύ υπάρχει σε δύο διακριτά πολύμορφα όταν βρίσκεται στην άνυδρη κατάστασή του. Όταν το οξαλικό οξύ μετατρέπεται στο πρώτο πολύμορφο, δημιουργείται δεσμός υδρογόνου. Είναι δυνατό να δημιουργηθεί μια δομή που μοιάζει με αλυσίδα σε διαμοριακό επίπεδο ως αποτέλεσμα αυτού του δεσμού υδρογόνου. Είναι επίσης πιθανό το δεύτερο πολύμορφο αυτής της χημικής ουσίας να υπόκειται σε δεσμούς υδρογόνου. Αλλά σε αυτό το συγκεκριμένο σενάριο, ο δεσμός υδρογόνου έχει ως αποτέλεσμα μια διαμοριακή δομή που είναι παρόμοια με μια δομή σαν φύλλο για το μόριο. Λόγω δύο σημαντικών χαρακτηριστικών αυτής της χημικής ουσίας, χρησιμοποιείται συνήθως σε αντιδράσεις εστεροποίησης. Η όξινη φύση του οξαλικού οξέος είναι το πρώτο χαρακτηριστικό που το καθιστά εξαιρετική επιλογή για διαδικασίες εστεροποίησης. Η υδρόφιλη φύση του οξαλικού οξέος είναι το δεύτερο και πιο ουσιαστικό χαρακτηριστικό της ένωσης.
Παρασκευή οξαλικού οξέος
Το οξαλικό οξύ μπορεί να παρασκευαστεί εύκολα με την οξείδωση ορισμένων υδατανθράκων, όπως η σακχαρόζη, παρουσία πυκνών διαλυμάτων νιτρικού οξέος. Το οξαλικό οξύ σχηματίζεται όταν τα άτομα άνθρακα σχίζονται σε ζεύγη κατά τη διάρκεια της διαδικασίας οξείδωσης.
Χρήσεις
- Χρησιμοποιείται ως μέσο στη διαδικασία βαφής
- Χρησιμοποιείται για την αφαίρεση σκουριάς
- Είναι ένα σημαντικό αντιδραστήριο στη χημεία των λανθανιδών και χρησιμοποιείται επίσης σε πολλούς άλλους τομείς
- Χρησιμοποιείται για το γυάλισμα μαρμάρινων αγαλμάτων για να τα κάνει να αστράφτουν
- Χρησιμοποιείται στην παραγωγή βαφών και στην παραγωγή λευκαντικών
- Χρησιμοποιείται στην αφαίρεση λεκέδων από τρόφιμα και μελάνι
- Χρησιμοποιείται στην ανάπτυξη φωτογραφικού φιλμ
- Χρησιμοποιείται στην επεξεργασία λυμάτων για την εξάλειψη των εναποθέσεων ασβεστίου που έχουν συσσωρευτεί με την πάροδο του χρόνου
Κίνδυνοι για την υγεία
Το οξαλικό οξύ είναι μια δηλητηριώδης ουσία. Ο έμετος, η διάρροια και οι σοβαρές γαστρεντερικές διαταραχές είναι μεταξύ των επικίνδυνων συμπτωμάτων που μπορεί να προκύψουν από την κατάποση. Άλλα συμπτώματα περιλαμβάνουν νεφρική βλάβη, σοκ, σπασμούς και κώμα. Η καρδιαγγειακή κατάρρευση έχει τη δυνατότητα να οδηγήσει σε θάνατο. Το οξαλικό οξύ είναι ένα ερεθιστικό του δέρματος που μπορεί να προκαλέσει ερεθισμό των ματιών, των βλεννογόνων και του δέρματος. Μπορεί να προκληθεί τραυματισμός νεφρού ως αποτέλεσμα εισπνοής ή κατάποσης.
Το οξαλικό οξύ είναι μια δηλητηριώδης ουσία. Η νεφρική βλάβη, το σοκ και οι σπασμοί είναι μερικές από τις επικίνδυνες παρενέργειες. Η τοξικότητα προκαλείται από το οξαλικό οξύ που αντιδρά με το ασβέστιο στους ιστούς για να δημιουργήσει οξαλικό ασβέστιο, το οποίο προκαλεί την αποβολή της αναλογίας καλίου ασβεστίου εκτός ισορροπίας. Η συσσώρευση οξαλικών στα νεφρικά σωληνάρια έχει τη δυνατότητα να προκαλέσει τραυματισμό των νεφρών.
Πονοκέφαλοι, ζάλη, ναυτία, έμετος, σπασμοί, κώμα, ακόμη και θάνατος μπορεί να εμφανιστούν ως αποτέλεσμα υπερβολικής δόσης οξαλικού οξέος σε ορισμένες περιπτώσεις. Η υπερβολική ή επαναλαμβανόμενη έκθεση στη χημική ουσία μπορεί να προκαλέσει δερματικό εξάνθημα, πόνο, ερυθρότητα, φουσκάλες και έλκη βραδείας επούλωσης, μεταξύ άλλων συμπτωμάτων.
Συμπέρασμα
Το οξαλικό οξύ βρίσκεται στα φυλλώδη χόρτα, στις φακές και στην πλειονότητα άλλων φυτικών τροφών. Το αποκτάτε μέσω της διατροφής σας επειδή είναι ένα φυσικό μόριο. Αποβάλλεται επίσης από τον οργανισμό ως απόβλητο. Οι τροφές πλούσιες σε οξαλικά περιέχουν επίσης μια ποικιλία από πρόσθετα θρεπτικά συστατικά που χρειάζεται το σώμα σας για βέλτιστη υγεία.
Όταν καταναλώνετε γεύματα που περιέχουν οξαλικό άλας, η χημική ουσία προσκολλάται σε μέταλλα, αναγκάζοντας τα μέταλλα να συνδυαστούν για να σχηματίσουν πρόσθετα μέταλλα. Ο οξαλικός σίδηρος και το οξαλικό ασβέστιο είναι παραδείγματα τέτοιων ενώσεων.
Οι δίαιτες χαμηλές σε οξαλικά άλατα μπορεί να είναι ωφέλιμες εάν έχετε υψηλό κίνδυνο παραγωγής πέτρας στα νεφρά ως αποτέλεσμα των υψηλών επιπέδων οξαλικών στο σώμα σας. Το μπρόκολο, το τυρί και τα κονσερβοποιημένα ψάρια με κόκαλα είναι παραδείγματα τέτοιων τροφών. Περιέχουν επίσης σημαντικές ποσότητες ασβεστίου.