Διαφορά μεταξύ εμπειρικού και μοριακού τύπου
Κύρια διαφορά – Εμπειρικός εναντίον μοριακού τύπου
Στη χημική βιβλιογραφία, ο όρος «τύπος» αναφέρεται στη γραπτή σύνθεση μιας ένωσης. Υπάρχουν διάφοροι τρόποι για την καταγραφή της σύνθεσης μιας ένωσης και έχουν διαφορετικές σημασίες. Η εμπειρική μορφή καταγραφής και η μοριακή μορφή καταγραφής είναι δύο τέτοιοι τρόποι. Η λέξη «εμπειρικό» σημαίνει ότι «τα αποτελέσματα λαμβάνονται πειραματικά». Ωστόσο, όταν εφαρμόζεται στο πλαίσιο ενός τύπου, ένας εμπειρικός τύπος είναι ο απλούστερος τύπος τύπου που χρησιμοποιείται για την έκφραση της σύνθεσης μιας ένωσης ενώ tο μοριακός τύπος είναι η ακριβής αναπαράσταση της πραγματικής ένωσης. Αυτή είναι η κύρια διαφορά μεταξύ εμπειρικού και μοριακού τύπου.
Τι είναι ένας εμπειρικός τύπος
Όπως αναφέρθηκε παραπάνω, αυτή είναι η απλούστερη μορφή ενός τύπου. Μόνο δίνει πληροφορίες για την αναλογία στην οποία υπάρχει κάθε στοιχείο στον τύπο έναντι των άλλων. Συνήθως, ο εμπειρικός τύπος αφαιρείται όταν η σύνθεση των στοιχείων στην ένωση παρουσιάζεται ως ποσοστά κατά βάρος. Επομένως, για να καταλήξουμε στον εμπειρικό τύπο, αυτό που πρέπει να γίνει είναι να υποθέσουμε ότι το συνολικό βάρος της ένωσης είναι 100 g. Με αυτόν τον τρόπο, κάθε ποσοστιαία ποσότητα μπορεί να μεταφραστεί απευθείας ως το στοιχειακό βάρος στην ένωση. Και μπορεί να γίνει σύγκριση των βαρών των στοιχείων σε γραμμάρια.
Ωστόσο, ο τύπος αναπαριστά τα στοιχεία σύμφωνα με τους στοιχειομετρικούς λόγους τους. Αυτό σημαίνει ότι τα βάρη πρέπει να μετατραπούν σε κρεατοελιές. Η μετατροπή μπορεί να επιτευχθεί με απλή διαίρεση κάθε βάρους σε γραμμάρια με το αντίστοιχο μοριακό βάρος (μονάδα ατομικής μάζας) του στοιχείου. Θα είχε ως αποτέλεσμα τον αριθμό των σπίλων που υπάρχουν για κάθε στοιχείο. Στη συνέχεια, αυτοί οι αριθμοί μπορούν να συγκριθούν ως αναλογίες και να απλοποιηθούν περαιτέρω μέχρι τον απλούστερο συνδυασμό αναλογιών. Αυτό που απομένει θα ήταν ο εμπειρικός τύπος για την εν λόγω ένωση.
Τι είναι ο μοριακός τύπος
Ο μοριακός τύπος σας δίνει την ακριβή στοιχειακή σύνθεση μιας ένωσης . Αυτή μπορεί να είναι η απλούστερη μορφή, που είναι ο εμπειρικός τύπος, ή ένα απλό πολλαπλάσιό της. Ο μοριακός τύπος θα είναι πάντα πολλαπλάσιο του εμπειρικού τύπου. Εάν όχι, θα θεωρηθεί σφάλμα.
Όταν βρίσκουμε τον μοριακό τύπο μιας ένωσης, είναι απαραίτητο το συνολικό βάρος της ένωσης (οι υποθέσεις όπως στην περίπτωση του εμπειρικού τύπου δεν ισχύουν εδώ). Και στη συνέχεια, το συνολικό βάρος που λαμβάνεται πρέπει να συγκριθεί με μια στοιχειακή κατανομή στον αριθμό των moles όπως δίνεται στον εμπειρικό τύπο και τα μοριακά βάρη κάθε στοιχείου. Επομένως, κάθε αριθμός γραμμομορίων ενός στοιχείου πολλαπλασιάζεται με το αντίστοιχο μοριακό του βάρος και προστίθενται μαζί. Στη συνέχεια, ολόκληρη αυτή η έκφραση πολλαπλασιάζεται με έναν ορισμένο «παράγοντα» και ισούται με το συνολικό βάρος που μετρήθηκε. Με αυτό, είναι δυνατό να βρεθεί η τιμή του «παράγοντα» που ενσωματώθηκε στην έκφραση στον πλησιέστερο ακέραιο αριθμό. Στη συνέχεια, αυτή η τιμή που βρέθηκε χρησιμοποιείται για να πολλαπλασιάσει τον αριθμό των γραμμομορίων κάθε στοιχείου στον εμπειρικό τύπο. Το αποτέλεσμα θα ήταν ο μοριακός τύπος της ένωσης.
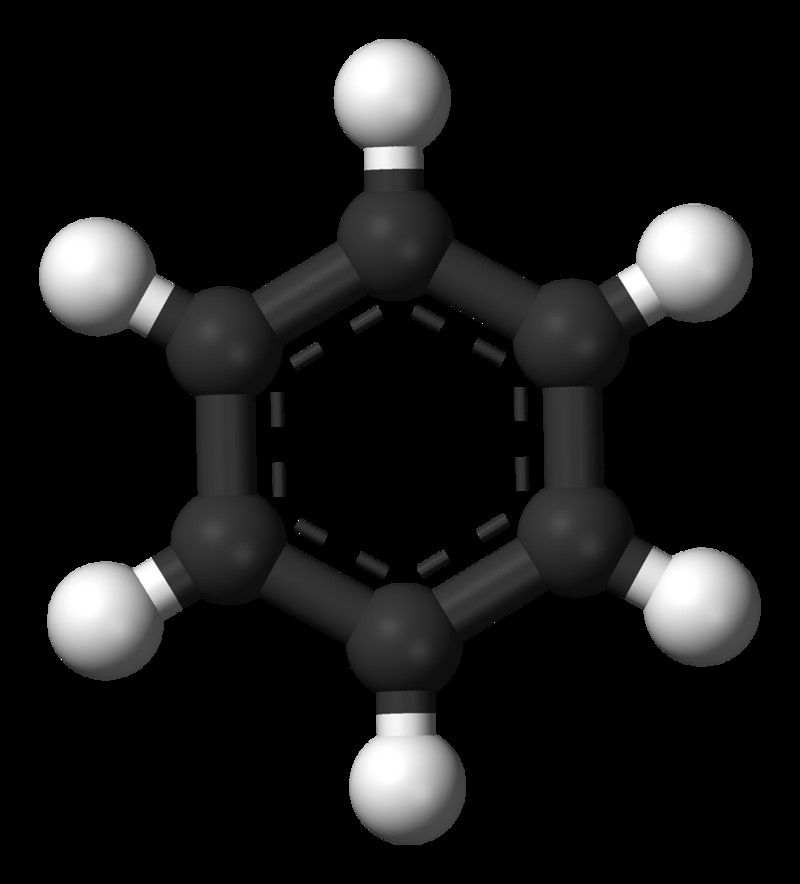
Ο εμπειρικός τύπος του βενζολίου είναι το CH. Ο μοριακός τύπος του βενζολίου είναι C6H6 .
Διαφορά μεταξύ εμπειρικού και μοριακού τύπου
Ορισμός
Εμπειρικός τύπος είναι η απλούστερη μορφή έκφρασης της στοιχειακής σύνθεσης μιας ένωσης.
Μοριακός τύπος είναι η πραγματική αναπαράσταση της στοιχειακής σύνθεσης της ένωσης.
Διαδικασία Παραγωγής
Ο εμπειρικός τύπος προέρχεται πρώτα από τα ποσοστά βάρους των στοιχείων που υπάρχουν στην ένωση.
Ο μοριακός τύπος σχετίζεται με το συνολικό βάρος της εν λόγω ένωσης και συχνά προκύπτει μετά την απόκτηση του εμπειρικού τύπου.
Σχέση μεταξύ εμπειρικού και μοριακού τύπου
Ο εμπειρικός τύπος περιέχει την πιο απλοποιημένη αναλογία των γραμμομορίων στοιχείων στην ένωση.
Ο μοριακός τύπος πρέπει να είναι πολλαπλάσιο του εμπειρικού τύπου.
Χρήση
Ο εμπειρικός τύπος δεν χρησιμοποιείται συχνά σε σχήματα αντίδρασης.
Ο μοριακός τύπος χρησιμοποιείται συνήθως σε αντιδράσεις και άλλες χημικές καταγραφές.
Ονοματολογία
Ο εμπειρικός τύπος δεν χρησιμοποιείται για σκοπούς ονομασίας, καθώς ένας εμπειρικός τύπος μπορεί να οδηγήσει σε οποιονδήποτε αριθμό μοριακών τύπων.
Ο μοριακός τύπος μιας ένωσης χρησιμοποιείται για την ονομασία του.





