Διαφορά μεταξύ νιτρικών και νιτρωδών
Κύρια διαφορά -Νιτρικά έναντι νιτρωδών
Τόσο τα νιτρικά όσο και τα νιτρώδη είναι ανόργανες χημικές ενώσεις και, όπως υποδηλώνουν τα ονόματα, το χαρακτηριστικό στοιχείο σε αυτές είναι "N" ή Άζωτο, που έχει ατομικό αριθμό 7. Το άζωτο είναι ένα άοσμο διατομικό αέριο στη φύση και είναι αντιδραστικό. Το στοιχείο Άζωτο είναι επίσης εξαιρετικά ηλεκτραρνητικό. Και τα νιτρικά και τα νιτρώδη είναι δύο σημαντικές κατηγορίες ενώσεων που περιέχουν άζωτο. Η κύρια διαφορά μεταξύ νιτρικών και νιτρωδών είναι ότι Η ομάδα νιτρικών περιέχει ένα άτομο αζώτου και τρία άτομα οξυγόνου λαμβάνοντας υπόψη ότι Η ομάδα νιτρωδών περιέχει ένα άτομο αζώτου και δύο άτομα οξυγόνου .
Τι είναι το νιτρικό άλας
Το νιτρικό είναι ένα πολυατομικό ιόν που αποτελείται από άτομα αζώτου και οξυγόνου. Η χημική δομή περιέχει ένα άτομο αζώτου και τρία άτομα οξυγόνου και αντιπροσωπεύεται από τον μοριακό τύπο NO3-. Η νιτρική ομάδα μπορεί να περιγραφεί ως λειτουργική ομάδα στην ανόργανη χημεία. Η ένωση έχει τριγωνική επίπεδη γεωμετρία. Αυτό μας λέει πώς τα άτομα μέσα στην ένωση είναι διατεταγμένα σε τρισδιάστατο χώρο. Σύμφωνα με τη δομή του νιτρικού, το άζωτο είναι το κέντρο και συνδέεται με τρία ίδια άτομα οξυγόνου. Ωστόσο, ανά πάσα στιγμή, μόνο ένα άτομο οξυγόνου συνδέεται διπλά με το κέντρο αζώτου, τα άλλα δύο άτομα οξυγόνου συνδέονται μέσω απλών δεσμών. Όμως, καθώς τα τρία άτομα οξυγόνου είναι πανομοιότυπα μεταξύ τους, πιστεύεται ότι η δομή είναι σύμφωνη με την αρχή του συντονισμού στη χημεία. Επομένως, προτείνει ότι ο διπλός δεσμός μπορεί να μεταναστεύσει μεταξύ οποιουδήποτε ατόμου οξυγόνου και του κέντρου αζώτου. Επίσης, το άζωτο έχει αριθμό οξείδωσης +5 στα νιτρικά.
Τα νιτρικά ιόντα έχουν συνολικό φορτίο -1, ωστόσο λαμβάνοντας υπόψη την κατανομή φορτίου εντός του ιόντος, το άτομο αζώτου φέρει φορτίο +1 και κάθε άτομο οξυγόνου φέρει φορτίο ίση με -(2/3), για να οδηγήσει σε συνολική χρέωση -1. Γενικά, όλα τα νιτρικά άλατα είναι διαλυτά στο νερό. Με το νερό, τα νιτρικά ιόντα σχηματίζουν νιτρικό οξύ, το οποίο θεωρείται ισχυρό οξύ. Οι νιτρικές ενώσεις χρησιμοποιούνται για λιπάσματα στη γεωργία, για την παραγωγή εκρηκτικών και πυροβόλων όπλων κ.λπ. 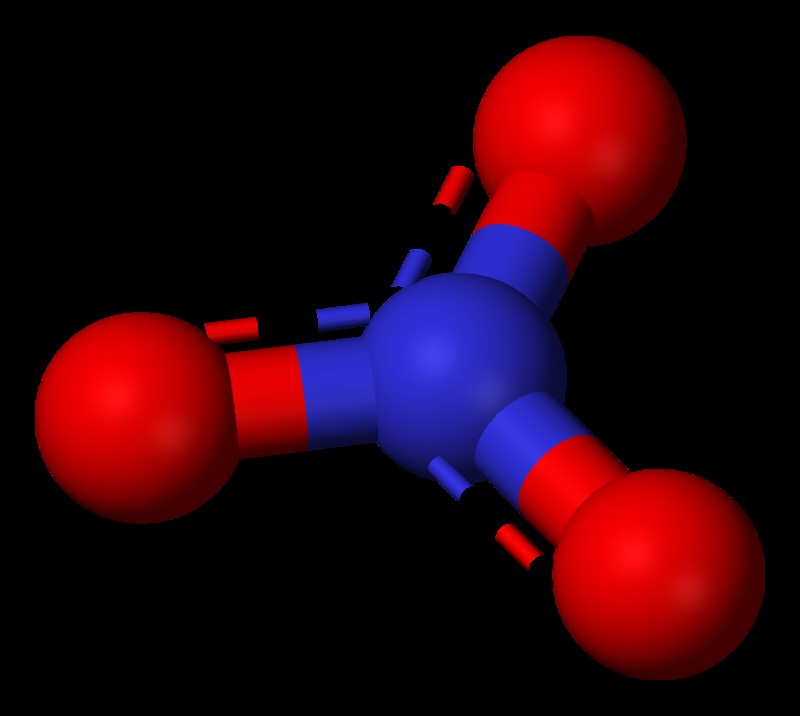
Τι είναι τα νιτρώδη
Τα νιτρώδη είναι επίσης ένα πολυατομικό ιόν που περιέχει άτομα Ν και Ο, όπου το άζωτο έχει αριθμό οξείδωσης +3. Η ομάδα νιτρωδών περιέχει ένα άτομο αζώτου και δύο άτομα οξυγόνου και αντιπροσωπεύεται από τον μοριακό τύπο, NO2-. Η γωνία δεσμού O-N-O είναι περίπου 120°. Αυτό μας δίνει μια ιδέα για το πώς τα άτομα είναι διατεταγμένα σε τρισδιάστατο χώρο. Τα νιτρώδη ιόντα μπορούν να οξειδωθούν για να σχηματίσουν νιτρικά άλατα καθώς ο αριθμός οξείδωσης του αζώτου στα νιτρώδη είναι μικρότερος από αυτόν των νιτρικών.
Κατά την αντίδραση με το νερό, τα νιτρώδη σχηματίζουν νιτρώδες οξύ, το οποίο θεωρείται ασθενές οξύ στην ανόργανη χημεία. Στη χημική δομή της ένωσης νιτρωδών, ένα άτομο οξυγόνου συνδέεται διπλά με το κέντρο του αζώτου και το άλλο συνδέεται μεμονωμένα. Ωστόσο, καθώς η αρχή του συντονισμού διέπει τη σχέση δομής της ομάδας, ο διπλός δεσμός μεταξύ του ατόμου οξυγόνου και του ατόμου αζώτου θεωρείται ότι μεταναστεύει συνεχώς. Ως εκ τούτου, τα δύο άτομα οξυγόνου θα έχουν την ίδια κατάσταση. Τα νιτρώδη παράγονται από νιτροποιητικά βακτήρια και χρησιμοποιούνται συχνά στη βιομηχανία τροφίμων για τη σκλήρυνση του κρέατος. Έχει επίσης σημαντικό βιοχημικό ρόλο ως αγγειοδιασταλτικό για το μονοξείδιο του αζώτου. 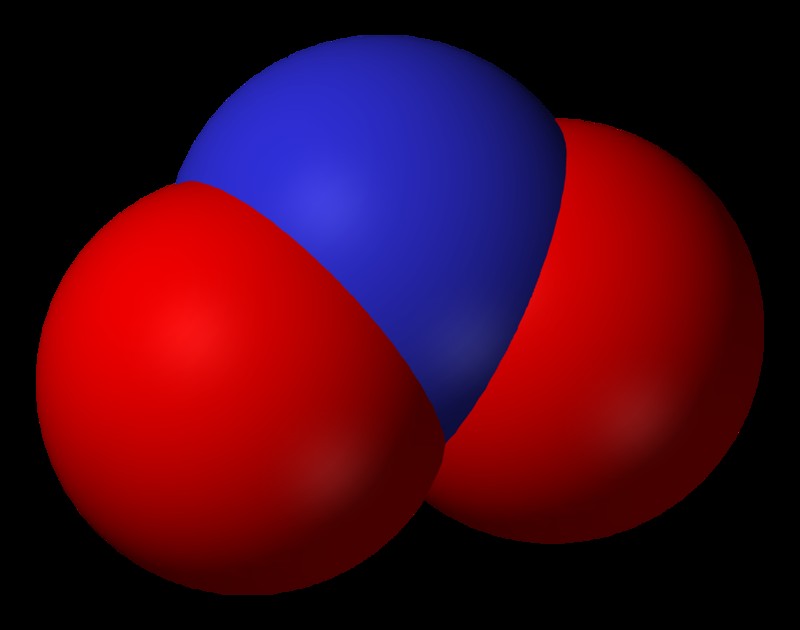
Διαφορά μεταξύ νιτρικών και νιτρωδών
Ορισμός
Νιτρικά είναι ένα ανόργανο πολυατομικό ιόν με φορτίο -1, κατασκευασμένο από ένα άτομο αζώτου και τρία άτομα οξυγόνου.
Νιτρώδη είναι ένα ανόργανο πολυατομικό ιόν με φορτίο -1, κατασκευασμένο από ένα άτομο αζώτου και δύο άτομα οξυγόνου.
Αριθμός οξείδωσης
Ο αριθμός οξείδωσης του Αζώτου σε Νιτρικά είναι +5.
Ο αριθμός οξείδωσης του Αζώτου σε Νιτρώδη είναι +3.
Μοριακό σχήμα
Νιτρικά άλατα έχουν τριγωνική επίπεδη γεωμετρία.
Νιτρώδη έχουν λυγισμένη μοριακή γεωμετρία.
Αντίδραση με νερό
Νιτρικά άλατα σχηματίζουν νιτρικό οξύ που είναι ισχυρό οξύ.
Νιτρώδη σχηματίζουν νιτρώδες οξύ που είναι ασθενές οξύ.
Οξείδωση και αναγωγή
Νιτρικά άλατα μπορεί να αναχθεί για να σχηματίσει νιτρώδη.
Νιτρώδη μπορεί να οξειδωθεί για να σχηματίσει νιτρικά άλατα. 
Ευγενική προσφορά εικόνας:
“Nitrate-3D-balls” του Benjah-bmm27 – Δική δουλειά. (Public Domain) μέσω Commons
"Nitrite-3D-vdW". (Public Domain) μέσω Commons




