Διαφορά μεταξύ γλυκόζης και σακχαρόζης
Κύρια διαφορά – Γλυκόζη έναντι Σακχαρόζης
Τόσο η γλυκόζη όσο και η σακχαρόζη είναι απλά σάκχαρα. Είναι ενώσεις με πολύ γλυκιά γεύση και διαλύονται καλά στο νερό. Αυτές οι ενώσεις έχουν διαφορετικές χρήσεις λόγω της γλυκύτητάς τους. Η κύρια διαφορά μεταξύ γλυκόζης και σακχαρόζης είναι ότι η γλυκόζη είναι μονοσακχαρίτης ενώ η σακχαρόζη είναι δισακχαρίτης. Ένας μονοσακχαρίτης εμφανίζεται ως ένα μόνο μόριο. Ένας δισακχαρίτης αποτελείται από δύο μόρια μονοσακχαρίτη που συνδέονται μεταξύ τους μέσω ενός γλυκοσιδικού δεσμού. Η σακχαρόζη είναι ένας δισακχαρίτης που αποτελείται από ένα μόριο γλυκόζης και ένα μόριο φρουκτόζης.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η Γλυκόζη
– Ορισμός, δομή, ιδιότητες και χρήσεις
2. Τι είναι η Σακχαρόζη
– Ορισμός, δομή, ιδιότητες και χρήσεις
3. Ποια είναι η διαφορά μεταξύ γλυκόζης και σακχαρόζης
– Σύγκριση βασικών διαφορών
Βασικοί όροι:δισακχαρίτης, φρουκτόζη, γλυκόζη, γλυκοσιδικός δεσμός, μονοσακχαρίτης, σακχαρόζη, ζάχαρη, γλυκύτητα 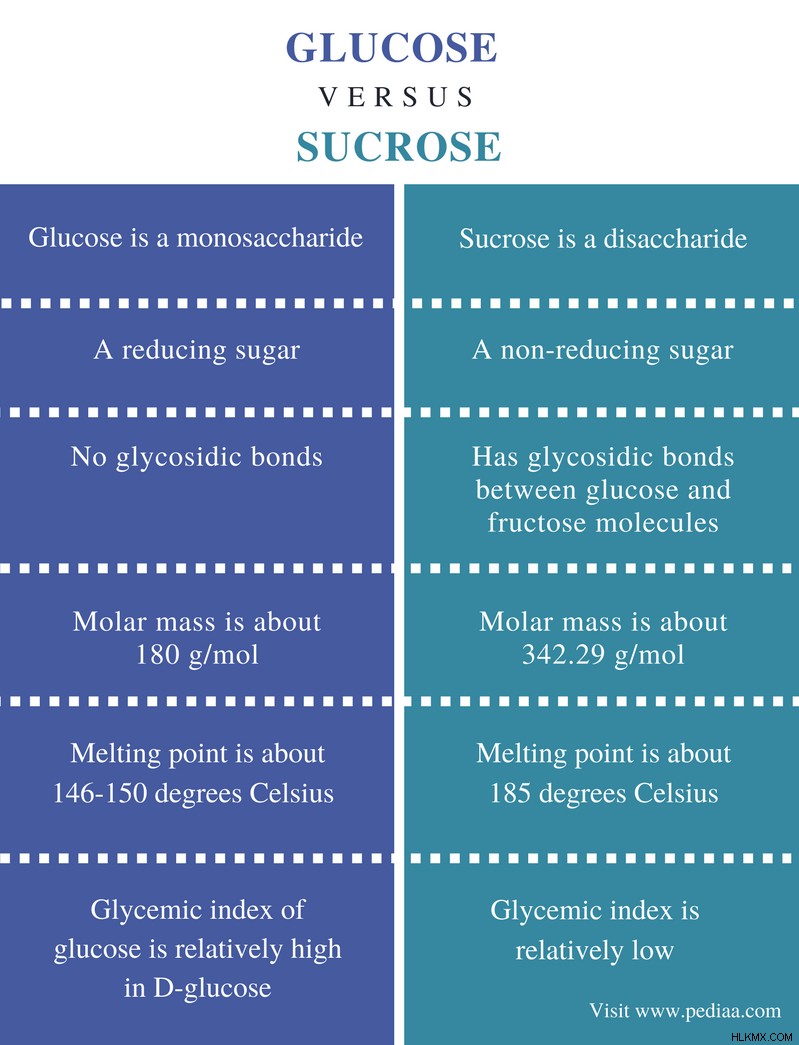
Τι είναι η γλυκόζη
Η γλυκόζη είναι ένα απλό σάκχαρο που έχει τον χημικό τύπο C6 H12 O6 . Είναι ένας μονοσακχαρίτης που είναι χρήσιμος στο σχηματισμό σημαντικών δισακχαριτών και πολυσακχαριτών. Η μοριακή μάζα της γλυκόζης είναι περίπου 180 g/mol. Εμφανίζεται ως λευκή σκόνη. Η γλυκόζη διαλύεται καλά στο νερό. Το σημείο τήξης αυτής της ένωσης κυμαίνεται από 146 C έως 150 C ανάλογα με τη χημική δομή του μορίου.
Η δομή της γλυκόζης μπορεί να δοθεί με διάφορες μορφές, όπως προβολή Fischer, προβολή Haworth και διαμόρφωση καρέκλας. Ας εξετάσουμε την προβολή Fischer που είναι πιο εύκολο να μελετηθεί. Η παρακάτω εικόνα δίνει την προβολή Fischer των δύο μορφών γλυκόζης. Η γλυκόζη μπορεί να βρεθεί με τις μορφές D-γλυκόζης ή L-γλυκόζης. Είναι εναντιομερή και είναι κατοπτρικές εικόνες το ένα του άλλου.
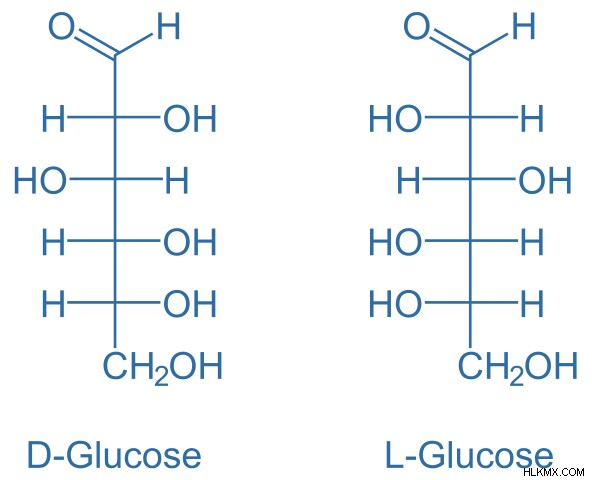
Εικόνα 1:Προβολή Fischer του μορίου γλυκόζης
Η πιο άφθονη μορφή είναι η D-γλυκόζη ενώ η L-γλυκόζη είναι λιγότερο άφθονη. Η D-γλυκόζη ονομάζεται επίσης δεξτρόζη, η οποία βρίσκεται ως συστατικό σε τρόφιμα που διατίθενται στο εμπόριο. Η γλυκόζη είναι μια σημαντική ένωση που χρησιμοποιείται στη βιομηχανία τροφίμων. έχει επίσης ιατρικές χρήσεις, όπως στην παραγωγή φαρμάκων για τη θεραπεία ασθενών με υπογλυκαιμία.
Οι πηγές γλυκόζης περιλαμβάνουν τους περισσότερους υδατάνθρακες που καταναλώνουμε. Εδώ, η γλυκόζη μπορεί να συμπεριληφθεί είτε σε μορφή μονοσακχαρίτη είτε ως δομικό στοιχείο πολυσακχαριτών. Η γλυκόζη είναι μια καλή πηγή ενέργειας για να αποκτήσουν ενέργεια οι αθλητές.
Τι είναι η σακχαρόζη
Η σακχαρόζη είναι ένα σάκχαρο δισακχαρίτη με χημικό τύπο C12 H22 O11 . Αποτελείται από δύο μόρια μονοσακχαρίτη. Είναι η γλυκόζη και η φρουκτόζη. Η σύνδεση μεταξύ αυτών των δύο μονοσακχαριτών ονομάζεται γλυκοσιδικός δεσμός. Η μοριακή μάζα της σακχαρόζης είναι περίπου 342,29 g/mol. Η σακχαρόζη είναι ένα μη αναγωγικό μόριο σακχάρου που βρίσκεται σε στερεή μορφή. Η σακχαρόζη είναι μια λευκή, άοσμη και κρυσταλλική στερεή ένωση.
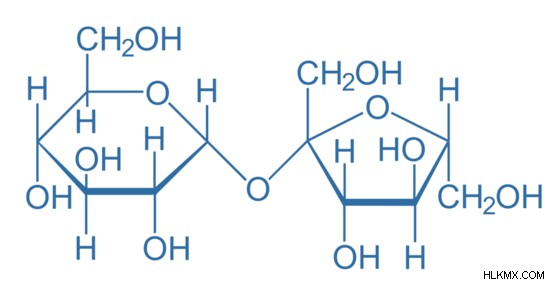
Εικόνα 2:Η χημική δομή της σακχαρόζης
Η κύρια πηγή σακχαρόζης είναι το ζαχαροκάλαμο. Το φυτό ζαχαροκάλαμου υποβάλλεται σε επεξεργασία για να ληφθεί σακχαρόζη με τη μορφή επιτραπέζιου αλατιού που καταναλώνουμε στην καθημερινή μας ζωή. Η σακχαρόζη έχει υψηλό βαθμό γλυκύτητας. Ως εκ τούτου, χρησιμοποιείται ως γλυκαντικό για αναψυκτικά και πολλά άλλα είδη διατροφής. Ωστόσο, ο γλυκαιμικός δείκτης της σακχαρόζης είναι συγκριτικά χαμηλός. Αυτό οφείλεται στην παρουσία 50% φρουκτόζης στη δομή της σακχαρόζης. Επομένως, η σακχαρόζη έχει ελάχιστη επίδραση στο σάκχαρο του αίματος.
Το σημείο τήξης της σακχαρόζης είναι περίπου 185C. Με περαιτέρω θέρμανση, η σακχαρόζη αποσυντίθεται σε ιμβερτοποιημένο σάκχαρο. Το ιμβερτοποιημένο σάκχαρο περιλαμβάνει μόρια γλυκόζης και φρουκτόζης. Επομένως, η αποσύνθεση της σακχαρόζης είναι η διάσπαση των μορίων σακχαρόζης σε γλυκόζη και φρουκτόζη.
Διαφορά μεταξύ γλυκόζης και σακχαρόζης
Ορισμός
Γλυκόζη: Η γλυκόζη είναι ένα απλό σάκχαρο που έχει τον χημικό τύπο C6 H12 O6 .
Σακχαρόζη: Η σακχαρόζη είναι ένα σάκχαρο δισακχαρίτη με χημικό τύπο C12 H22 O11 .
Φύση του μορίου
Γλυκόζη: Η γλυκόζη είναι ένας μονοσακχαρίτης.
Σακχαρόζη: Η σακχαρόζη είναι δισακχαρίτης.
Μείωση
Γλυκόζη: Η γλυκόζη είναι ένα αναγωγικό σάκχαρο.
Σακχαρόζη: Η σακχαρόζη είναι ένα μη αναγωγικό σάκχαρο.
Γλυκοσιδικός δεσμός
Γλυκόζη: Η γλυκόζη δεν έχει γλυκοσιδικούς δεσμούς.
Σακχαρόζη: Η σακχαρόζη έχει γλυκοζιτικούς δεσμούς μεταξύ των μορίων γλυκόζης και φρουκτόζης.
Μοριακή μάζα
Γλυκόζη: Η μοριακή μάζα της γλυκόζης είναι περίπου 180 g/mol.
Σακχαρόζη: Η μοριακή μάζα της σακχαρόζης είναι περίπου 342,29 g/mol.
Σημείο τήξης
Γλυκόζη: Το σημείο τήξης της γλυκόζης είναι περίπου 146-150 C.
Σακχαρόζη: Το σημείο τήξης της σακχαρόζης είναι περίπου 185 C.
Γλυκαιμικός Δείκτης
Γλυκόζη: Ο γλυκαιμικός δείκτης της γλυκόζης είναι σχετικά υψηλός σε D-γλυκόζη.
Σακχαρόζη: Ο γλυκαιμικός δείκτης είναι σχετικά χαμηλός σε σακχαρόζη.
Συμπέρασμα
Η γλυκόζη και η σακχαρόζη είναι πολύ κοινές μορφές σακχάρων. Είναι ενώσεις με γλυκιά γεύση. Ως εκ τούτου, αυτές οι ενώσεις χρησιμοποιούνται ως γλυκαντικά στη βιομηχανία τροφίμων. Ωστόσο, αυτά τα σάκχαρα διαφέρουν μεταξύ τους ανάλογα με τη χημική τους δομή και άλλες ιδιότητες. Η βασική διαφορά μεταξύ της γλυκόζης και της σακχαρόζης είναι ότι η γλυκόζη είναι μονοσακχαρίτης ενώ η σακχαρόζη είναι δισακχαρίτης.




