Ποια είναι η δομή συγκόλλησης του νατρίου;
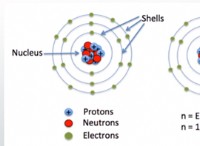
Το νάτριο έχει ατομικό αριθμό 11, που σημαίνει ότι έχει 11 πρωτόνια και 11 ηλεκτρόνια. Τα πρώτα δέκα ηλεκτρόνια γεμίζουν τα δύο πρώτα επίπεδα ενέργειας, ενώ το ενδέκατο ηλεκτρόνιο είναι το ηλεκτρόνιο σθένους. Αυτό σημαίνει ότι το νάτριο είναι μέταλλο και συνδέεται με τη δωρεά ηλεκτρονίου σθένους σε άλλα άτομα.
Όταν οι δεσμοί νατρίου με ένα άλλο άτομο, τα δύο άτομα συγκρατούνται από ιοντικό δεσμό. Αυτό οφείλεται στο γεγονός ότι το άτομο νατρίου δίνει το ηλεκτρόνιο του στο άλλο άτομο, το οποίο έχει ως αποτέλεσμα ένα θετικό ιόν και ένα αρνητικό ιόν. Τα θετικά και αρνητικά ιόντα στη συνέχεια προσελκύονται μεταξύ τους και αυτό το αξιοθέατο τα συγκρατεί.
Δεσμοί νατρίου με μια ποικιλία άλλων ατόμων, συμπεριλαμβανομένου του χλωρίου, του φθορίου, του οξυγόνου και του θείου. Αυτοί οι δεσμοί είναι όλοι ιοντικοί δεσμοί και όλοι οδηγούν στο σχηματισμό θετικού ιόντος νατρίου και ενός αρνητικού ιόντος του άλλου ατόμου.
Το νάτριο συνδέεται επίσης με τον εαυτό του για να σχηματίσει ένα μεταλλικό πλέγμα. Σε ένα μεταλλικό πλέγμα, τα άτομα νατρίου είναι διατεταγμένα σε κανονικό πρότυπο και όλα συνδέονται μεταξύ τους με ιοντικούς δεσμούς. Το μεταλλικό πλέγμα είναι υπεύθυνο για τις χαρακτηριστικές ιδιότητες του νατρίου, όπως η υψηλή ηλεκτρική και θερμική αγωγιμότητα του.