Διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου
Κύρια διαφορά – Υπεροξείδιο έναντι υπεροξειδίου
Οξείδιο είναι κάθε χημική ένωση που περιέχει ένα ή περισσότερα άτομα οξυγόνου. Τα οξείδια μπορεί να είναι οξείδια που περιέχουν ανιόντα οξειδίου (O), υπεροξείδια που περιέχουν ανιόντα υπεροξειδίου (O) ή υπεροξείδια που περιέχουν ανιόντα υπεροξειδίου (O2 ). Υπεροξείδιο είναι οποιαδήποτε ένωση που αποτελείται από έναν απλό δεσμό οξυγόνου-οξυγόνου. Αυτό μπορεί να είναι είτε με τη μορφή ενός ανιόντος είτε μεταξύ άλλων ατόμων του μορίου. Το υπεροξείδιο του υδρογόνου είναι το απλούστερο υπεροξείδιο που μπορεί να βρεθεί. Το υπεροξείδιο αποτελείται από εξαιρετικά δραστικά άτομα οξυγόνου. Τα υπεροξείδια σχηματίζονται μόνο από αλκαλικά μέταλλα (στοιχεία της ομάδας 1). Η κύρια διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου είναι ότι η κατάσταση οξείδωσης του οξυγόνου στο υπεροξείδιο είναι -1 ενώ η κατάσταση οξείδωσης του οξυγόνου στο υπεροξείδιο είναι -1/2.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το υπεροξείδιο
– Ορισμός, Δομή, Παραδείγματα
2. Τι είναι το υπεροξείδιο
– Ορισμός, Δομή, Παραδείγματα
3. Ποια είναι η διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου
– Σύγκριση βασικών διαφορών
Βασικοί όροι:μέταλλο αλκαλίων, μέταλλα αλκαλικών γαιών, ανιόν, μήκος δεσμού, μέταλλα, μη μέταλλα, οξείδιο, υπεροξείδιο, ανιόν υπεροξειδίου, υπεροξο, υπεροξείδιο
Τι είναι το υπεροξείδιο
Υπεροξείδιο είναι οποιαδήποτε ένωση που αποτελείται από έναν απλό δεσμό οξυγόνου-οξυγόνου. Επομένως, το κύριο χαρακτηριστικό για την αναγνώριση μιας ένωσης υπεροξειδίου είναι η παρουσία αυτού του ομοιοπολικού δεσμού Ο-Ο. Μερικές φορές, αυτός ο δεσμός μπορεί να παρατηρηθεί ως ανιόν σε μια ιοντική ένωση. Στη συνέχεια δίνεται σε σύμβολα ως O2 . Αυτό ονομάζεται ανιόν υπεροξειδίου . Όταν ο δεσμός Ο-Ο βρίσκεται σε μια ομοιοπολική ένωση, ονομάζεται υπεροξοομάδα ή ομάδα υπεροξειδίου.

Εικόνα 1:H2 O2 είναι το απλούστερο υπεροξείδιο
Στην ομάδα υπεροξειδίου, η κατάσταση οξείδωσης ενός ατόμου οξυγόνου είναι -1. Κανονικά το οξυγόνο προτιμά να δείχνει την κατάσταση οξείδωσης 0 ή -2. Αλλά επειδή δύο άτομα οξυγόνου συνδέονται μεταξύ τους, ένα άτομο οξυγόνου παίρνει κατάσταση οξείδωσης -1. Στο ανιόν υπεροξειδίου, ένα άτομο οξυγόνου έχει -1 ηλεκτρικό φορτίο αφού το συνολικό φορτίο του ανιόντος είναι -2.
Τα ιοντικά υπεροξείδια αποτελούνται από ένα ανιόν υπεροξειδίου συνδεδεμένο με ιόντα μετάλλων αλκαλίων ή ιόντα μετάλλου αλκαλικής γαίας ως κατιόν. Μερικά παραδείγματα είναι το υπεροξείδιο του νατρίου (Na2 O2 ), υπεροξείδιο του καλίου (K2 O2 ), υπεροξείδιο του μαγνησίου (MgO), κ.λπ. Οι ομοιοπολικές ενώσεις υπεροξειδίου αποτελούνται από απλό δεσμό Ο-Ο που συνδέεται άμεσα με άλλα άτομα του μορίου. για παράδειγμα, υπεροξείδιο του υδρογόνου (H2 O2 ) και υπεροξυμονοθειικό οξύ (H2 SO5 ).
Τα υπεροξείδια μπορούν να βρεθούν σε βιολογικά συστήματα και στη φύση. Για παράδειγμα, ορισμένα ένζυμα στα κύτταρά μας χρησιμοποιούν υπεροξείδια για να καταλύσουν ορισμένες αντιδράσεις. Ορισμένα είδη φυτών χρησιμοποιούν ενώσεις υπεροξειδίου ως χημικές ουσίες σηματοδότησης. Τα υπεροξείδια χρησιμοποιούνται επίσης σε εφαρμογές εργαστηριακής κλίμακας. Είναι πολύ χρήσιμο στην οργανική χημεία προκειμένου να ληφθεί το προϊόν anti-Markovnikov από μια οργανική αντίδραση.
Τι είναι το Superoxide
Τα υπεροξείδια είναι ενώσεις που περιέχουν το ανιόν O2 . Στην ομάδα του υπεροξειδίου, η κατάσταση οξείδωσης ενός ατόμου οξυγόνου είναι -1/2. Κανονικά το οξυγόνο προτιμά να δείχνει την κατάσταση οξείδωσης 0 ή -2. Αλλά επειδή υπάρχουν δύο άτομα οξυγόνου που συνδέονται μεταξύ τους, ένα άτομο οξυγόνου παίρνει κατάσταση οξείδωσης -1/2. Στο ανιόν υπεροξειδίου , ένα άτομο οξυγόνου έχει -1/2 ηλεκτρικό φορτίο αφού το συνολικό φορτίο του ανιόντος είναι -1.
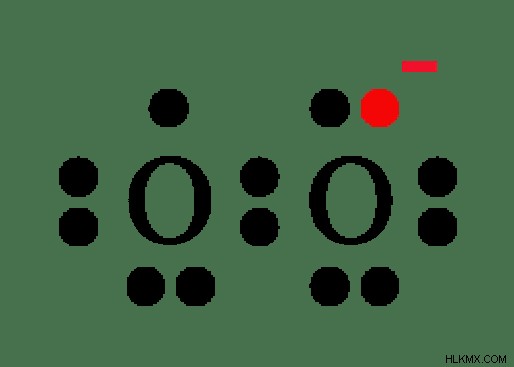
Εικόνα 2:Χημική δομή ανιόντος υπεροξειδίου
Αυτό το ανιόν αποτελείται επίσης από απλό δεσμό O-O. Το ανιόν υπεροξειδίου είναι πολύ αντιδραστικό επειδή η κατάσταση οξείδωσης -1/2 δεν είναι σταθερή. Το ανιόν υπεροξειδίου θεωρείται ως μια ελεύθερη ρίζα που εμφανίζει παραμαγνητισμό. Αυτό οφείλεται στην παρουσία ενός μη ζευγαρωμένου ηλεκτρονίου σε ένα άτομο οξυγόνου (όπως φαίνεται στην παραπάνω εικόνα).
Η απόσταση δεσμού για τον δεσμό O-O σε ανιόν υπεροξειδίου είναι περίπου 1,33Α. Μόνο τα αλκαλικά μέταλλα τείνουν να σχηματίζουν ενώσεις υπεροξειδίου. Σχηματίζουν την ένωση υπεροξειδίου μέσω άμεσης αντίδρασης με το O2 . Τα υπεροξείδια των αλκαλιμετάλλων περιλαμβάνουν το NaO2 , KO2 , RbO2 και CsO2 . Εδώ, το μέταλλο έχει +1 ηλεκτρικό φορτίο. Αντίστοιχα, το ανιόν θα πρέπει να έχει -1 ηλεκτρικό φορτίο για να εξουδετερώσει την ένωση.
Όταν αυτές οι ενώσεις υπεροξειδίου διαλύονται στο νερό, το σύστημα υφίσταται δυσαναλογία γρήγορα. Η δυσαναλογία είναι μια αντίδραση οξειδοαναγωγής στην οποία μια ένωση ενδιάμεσης κατάστασης οξείδωσης μετατρέπεται σε δύο διαφορετικές ενώσεις. Εδώ, ανιόν υπεροξειδίου και νερό αντιδρούν για να σχηματίσουν O2 και ιόν ΟΗ.
4O2 + 2H2 O → 3O2 + 4OH
Αυτή η αντίδραση είναι ο λόγος που το υπεροξείδιο του καλίου χρησιμοποιείται ως πηγή οξυγόνου σε χημικές γεννήτριες οξυγόνου σε διαστημικά λεωφορεία και υποβρύχια.
Διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου
Ορισμός
Υπεροξείδιο: Υπεροξείδιο είναι οποιαδήποτε ένωση που αποτελείται από έναν απλό δεσμό οξυγόνου-οξυγόνου.
Υπεροξείδιο: Τα υπεροξείδια είναι ενώσεις που περιέχουν το ανιόν O2 .
Χημικός τύπος
Υπεροξείδιο: Ο χημικός τύπος του ανιόντος υπεροξειδίου είναι O2 .
Υπεροξείδιο: Ο χημικός τύπος του ανιόντος υπεροξειδίου είναι O2 .
Ηλεκτρική φόρτιση
Υπεροξείδιο: Το ηλεκτρικό φορτίο του ιόντος υπεροξειδίου είναι -2.
Υπεροξείδιο: Το ηλεκτρικό φορτίο του ιόντος υπεροξειδίου είναι -1.
Μήκος δεσμού
Υπεροξείδιο: Το μήκος του δεσμού O-O σε ιόν υπεροξειδίου είναι 1,49°A.
Υπεροξείδιο: Το μήκος του δεσμού O-O σε ιόν υπεροξειδίου είναι 1,33°A.
Φύση
Υπεροξείδιο: Μέταλλα (όπως αλκαλιμέταλλα) και αμέταλλα (όπως το υδρογόνο) μπορούν να σχηματίσουν ενώσεις υπεροξειδίου.
Υπεροξείδιο: Μόνο τα αλκαλικά μέταλλα μπορούν να σχηματίσουν ενώσεις υπεροξειδίου.
Παραδείγματα
Υπεροξείδιο: Παραδείγματα για ενώσεις υπεροξειδίου περιλαμβάνουν το Na2O2 , K2O2 , Rb2O2 και Cs2O2
Υπεροξείδιο: Παραδείγματα για ενώσεις υπεροξειδίου περιλαμβάνουν το NaO2 , KO2 , RbO2 και CsO2.
Συμπέρασμα
Το υπεροξείδιο και το υπεροξείδιο είναι οξείδια που περιέχουν άτομα οξυγόνου. Η κύρια διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου είναι ότι η κατάσταση οξείδωσης του οξυγόνου στο υπεροξείδιο είναι -1 ενώ η κατάσταση οξείδωσης του οξυγόνου στο υπεροξείδιο είναι -1/2.
Αναφορά:
1. "12.4:Υπεροξείδια και υπεροξείδια." Chemistry LibreTexts, Libretexts, 21 Ιουλίου 2016, Διαθέσιμο εδώ.
2. "Superoxide." Wikipedia, Ίδρυμα Wikimedia, 15 Δεκεμβρίου 2017, Διαθέσιμο εδώ.
Εικόνα Ευγενική προσφορά:
1. «Δομή αερίου H2O2» Από SVG:Sassospicco; Raster:Walkerma – Αρχείο:H2O2 structure.png (GFDL) μέσω Commons Wikimedia
2. "Superoxide" (Δημόσιος Τομέας) μέσω Commons Wikimedia




