Τι έχει η μεγαλύτερη ηλεκτροαρνητικότητα h cl o f na;
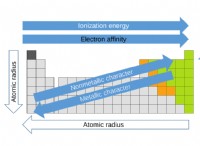
Η ηλεκτροαρνητικότητα αυξάνεται γενικά από αριστερά προς τα δεξιά κατά τη διάρκεια μιας περιόδου (σειρά) και μειώνεται από πάνω προς τα κάτω μέσα σε μια ομάδα (στήλη) στον περιοδικό πίνακα. Το φθόριο βρίσκεται στην επάνω δεξιά γωνία του περιοδικού πίνακα, γεγονός που το καθιστά το πιο ηλεκτροαρνητικό στοιχείο μεταξύ των συγκεκριμένων επιλογών.