Μήπως η οξύτητα ενός διαλύματος αντικατοπτρίζει τα ελεύθερα ιόντα υδρογόνου σε διάλυμα;
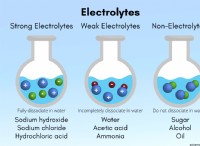
Όταν ένα οξύ διαλύεται σε νερό, απελευθερώνει ιόντα υδρογόνου, αυξάνοντας τη συγκέντρωση Η+ στο διάλυμα. Αυτή η αύξηση των ιόντων υδρογόνου καθιστά το διάλυμα πιο όξινο. Τα περισσότερα ιόντα υδρογόνου που υπάρχουν, τόσο ισχυρότερη είναι η οξύτητα. Αντίθετα, μια βάση, όταν διαλύεται σε νερό, απελευθερώνει ιόντα υδροξειδίου (OH-), τα οποία συνδυάζονται με ιόντα υδρογόνου για να σχηματίσουν μόρια νερού, μειώνοντας τη συγκέντρωση Η+ και καθιστώντας το διάλυμα λιγότερο όξινο ή πιο βασικό.
Η κλίμακα pH είναι μια λογαριθμική κλίμακα που κυμαίνεται από 0 έως 14, πού:
- Το ρΗ <7 υποδεικνύει ένα όξινο διάλυμα με υψηλή συγκέντρωση ιόντων υδρογόνου.
- Το ρΗ =7 υποδεικνύει ένα ουδέτερο διάλυμα με ίσες συγκεντρώσεις ιόντων υδρογόνου και ιόντων υδροξειδίου.
- Το PH> 7 υποδεικνύει ένα βασικό ή αλκαλικό διάλυμα με χαμηλή συγκέντρωση ιόντων υδρογόνου.
Η οξύτητα ενός διαλύματος επηρεάζει διάφορες χημικές αντιδράσεις και διαδραματίζει κρίσιμο ρόλο σε πολλές βιολογικές διεργασίες. Η κατανόηση και ο έλεγχος της οξύτητας είναι απαραίτητη σε τομείς όπως η χημεία, η βιολογία, η ιατρική και η περιβαλλοντική επιστήμη.