Περιγράφει ένα μόριο στο οποίο διαχωρίζονται τα θετικά και αρνητικά φορτία;
Τα πολικά μόρια σχηματίζονται όταν τα άτομα που συνθέτουν το μόριο έχουν διαφορετικές ηλεκτροθερμικές ικανότητες. Η ηλεκτροαρνητικότητα είναι ένα μέτρο της ικανότητας ενός ατόμου να προσελκύει ηλεκτρόνια. Όταν δύο άτομα με διαφορετικό δεσμό ηλεκτροναριναρίων, το πιο ηλεκτροαρνητικό άτομο θα προσελκύσει τα ηλεκτρόνια πιο έντονα, δημιουργώντας ένα μερικό αρνητικό φορτίο στον εαυτό του και ένα μερικό θετικό φορτίο στο άλλο άτομο.
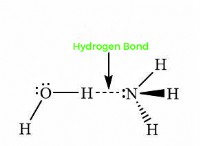
Η πολικότητα ενός μορίου μπορεί επίσης να επηρεαστεί από το σχήμα του μορίου. Ένα συμμετρικό μόριο, όπως το διοξείδιο του άνθρακα, δεν έχει καθαρή διπολική στιγμή επειδή τα θετικά και αρνητικά φορτία κατανέμονται ομοιόμορφα. Ωστόσο, ένα ασύμμετρο μόριο, όπως το νερό, έχει μια καθαρή ροπή διπολικής επειδή τα θετικά και αρνητικά φορτία διαχωρίζονται.
Τα πολικά μόρια είναι σημαντικά επειδή μπορούν να αλληλεπιδρούν μεταξύ τους μέσω αλληλεπιδράσεων διπολικής διπόλης. Αυτές οι αλληλεπιδράσεις είναι υπεύθυνες για τη συνοχή των πολικών υγρών και τη διαλυτότητα των πολικών ουσιών σε πολικούς διαλύτες. Τα πολικά μόρια διαδραματίζουν επίσης σημαντικό ρόλο στα βιολογικά συστήματα, όπου εμπλέκονται σε μια ποικιλία αλληλεπιδράσεων, όπως η δέσμευση υδρογόνου και η ιοντική δέσμευση.