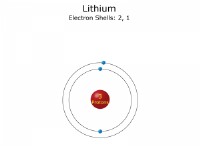
Γιατί το λίθιο και το βηρυλλικό ομοιοπολικό στη φύση;
Ο ομοιοπολικός χαρακτήρας ενός δεσμού καθορίζεται από τη διαφορά στην ηλεκτροαρνητικότητα μεταξύ των συνδεδεμένων ατόμων. Όσο μεγαλύτερη είναι η διαφορά στην ηλεκτροαρνητικότητα, τόσο πιο ιοντική είναι ο δεσμός. Το λίθιο και το βηρύλλιο έχουν σχετικά χαμηλές ηλεκτροαναγκεύσεις, έτσι ώστε οι δεσμοί που σχηματίζονται με άλλα στοιχεία είναι πιο ιοντικά από το ομοιοπολικό.