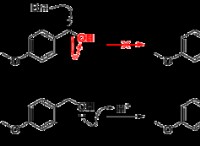
Επίδραση του υδροχλωρικού οξέος στο άμυλο;
- Πρωτονία:Το διάλυμα HCl, που είναι όξινο, δωρίζει ιόντα υδρογόνου (Η+) στα μόρια αμύλου. Αυτά τα ιόντα Η+ συνδέονται με τα άτομα οξυγόνου που υπάρχουν στις ομάδες υδροξυλίου του αμύλου (-OH).
- διάσπαση των γλυκοσιδικών δεσμών:Μόλις οι ομάδες υδροξυλίου πρωτονιωθούν, τα ιόντα υδρογόνου που υπάρχουν διευκολύνουν τη διάσπαση των γλυκοσιδικών δεσμών που συνδέουν τις μονάδες γλυκόζης στα μόρια αμύλου. Αυτή η θραύση του δεσμού χωρίζει το άμυλο σε μικρότερες μονάδες μόριας γλυκόζης.
- Ο σχηματισμός των δεξτρίνων:Αρχικά, η διάσπαση του αμύλου οδηγεί στο σχηματισμό ενδιάμεσων προϊόντων που ονομάζονται δεξτρίνες. Οι δεξτρίνες είναι μικρότεροι σύνθετοι υδατάνθρακες που αποτελούνται από σύντομες αλυσίδες μονάδων γλυκόζης που συνδέονται ακόμα μαζί.
- Περαιτέρω υδρόλυση:Καθώς προχωρά η αντίδραση, οι δεξτρίνες διασπώνται περαιτέρω σε μεμονωμένα μόρια γλυκόζης. Η διάσπαση συνεχίζεται έως ότου το μεγαλύτερο μέρος του αμύλου έχει μετατραπεί σε γλυκόζη.
Συνολικά, η επίδραση του υδροχλωρικού οξέος στο άμυλο είναι να σπάσει τα σύνθετα μόρια αμύλου σε απλά μόρια γλυκόζης μέσω της διαδικασίας υδρόλυσης. Αυτός ο μετασχηματισμός μπορεί να είναι χρήσιμος σε διάφορες βιομηχανικές εφαρμογές, όπως η παραγωγή σιροπιού γλυκόζης, διεργασίες ζύμωσης και κατασκευής κλωστοϋφαντουργικών προϊόντων.