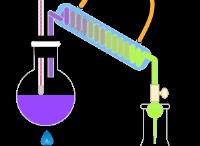
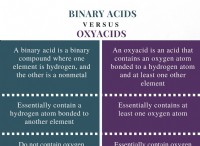
Είναι επίσης μια εξαιρετικά εύφλεκτη ουσία ουσία;
καύσιμο αναφέρεται στην ευκολία με την οποία μια ουσία αναφλέγεται και καίει. Αυτό καθορίζεται σε μεγάλο βαθμό από το:
* σημείο φλας: Τη χαμηλότερη θερμοκρασία στην οποία μια ουσία εκπέμπει αρκετούς ατμούς για ανάφλεξη.
* Θερμοκρασία ανάφλεξης: Η ελάχιστη θερμοκρασία που απαιτείται για την έναρξη της καύσης χωρίς εξωτερική πηγή ανάφλεξης.
Αντιδραστικότητα Περιγράφει πόσο εύκολα μια ουσία υφίσταται χημική αλλαγή, ειδικά σε σχέση με άλλες ουσίες. Αυτό μπορεί να περιλαμβάνει:
* Οξείδωση: Αντίδραση με οξυγόνο, το οποίο μπορεί να απελευθερώσει θερμότητα και να είναι εκρηκτική.
* Αντιδράσεις οξειδοαναγωγής: Αντιδράσεις που περιλαμβάνουν τη μεταφορά ηλεκτρονίων.
* αποσύνθεση: Διασπάται σε απλούστερες ουσίες.
Εδώ είναι η σύνδεση:
* Πολλές εξαιρετικά εύφλεκτες ουσίες είναι αντιδραστικές: Αντιδρούν εύκολα με οξυγόνο, συχνά με γρήγορο και εξώθερμο τρόπο, προκαλώντας καύση. Αυτός είναι ο λόγος για τον οποίο τα εύφλεκτα υγρά όπως η βενζίνη είναι εξαιρετικά αντιδραστικά με οξυγόνο.
* Όλες οι αντιδραστικές ουσίες δεν είναι εξαιρετικά εύφλεκτες: Ορισμένες ουσίες μπορούν να αντιδράσουν εύκολα χωρίς να εμπλέκουν φωτιά. Για παράδειγμα, το νάτριο αντιδρά έντονα με το νερό, παράγοντας θερμότητα και υδρογόνο, αλλά αυτή η αντίδραση δεν θεωρείται καύση.
Παραδείγματα:
* εξαιρετικά εύφλεκτο και αντιδραστικό: Διαιθυλαιθέρα, βενζίνη, μεθάνιο
* εξαιρετικά εύφλεκτο, αλλά όχι απαραίτητα εξαιρετικά αντιδραστικό: Ξύλο, χαρτί (η καύση είναι μια σύνθετη αντίδραση με οξυγόνο, αλλά όχι απαραίτητα μια "αντιδραστική" ουσία με τη χημική έννοια)
* αντιδραστική, αλλά όχι εξαιρετικά καύσιμα: Μέταλλο νατρίου (αντιδρά βίαια με νερό, αλλά δεν καίγεται)
Συνοπτικά:
Η εύκαμπτη δυνατότητα και η αντιδραστικότητα είναι σχετικές έννοιες αλλά όχι συνώνυμες. Ενώ πολλές καύσιμες ουσίες είναι αντιδραστικές, δεν είναι όλες οι αντιδραστικές ουσίες.