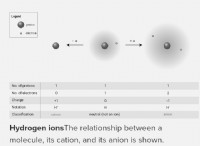
Πώς σχετίζονται τα emprical και τα μοριακά σχήματα για μια ένωση;
* Εμπειρική φόρμουλα: Αντιπροσωπεύει την απλούστερη αναλογία ατόμων σε μια ένωση. Σας λέει το είδος των παρόντων ατόμων και των σχετικών αναλογιών τους.
* Μοριακός τύπος: Αντιπροσωπεύει τον πραγματικό αριθμό ατόμων κάθε στοιχείου σε ένα μόριο της ένωσης.
Εδώ είναι η βασική σχέση:
* Η μοριακή φόρμουλα είναι πάντα ένα πολλαπλάσιο πλήρους αριθμού της εμπειρικής φόρμουλας.
Παράδειγμα:
* γλυκόζη:
* Εμπειρική φόρμουλα: Ch₂o (αυτή είναι η απλούστερη αναλογία ατόμων άνθρακα, υδρογόνου και οξυγόνου)
* Μοριακός τύπος: C₆h₁₂o₆ (αυτός είναι ο πραγματικός αριθμός ατόμων σε ένα μόριο γλυκόζης)
Για να φτάσετε από εμπειρική φόρμουλα σε μοριακό τύπο, χρειάζεστε:
1. Η εμπειρική φόρμουλα: Αυτό σας λέει τις βασικές αναλογίες ατόμων.
2. Η μοριακή μάζα της ένωσης: Αυτό σας λέει την πραγματική μάζα ενός μορίου.
Εδώ μπορείτε να βρείτε τη μοριακή φόρμουλα:
1. Υπολογίστε την εμπειρική μάζα τύπου: Προσθέστε τις ατομικές μάζες των ατόμων στον εμπειρικό τύπο.
2. Διαιρέστε τη μοριακή μάζα της ένωσης από την εμπειρική μάζα τύπου: Αυτό σας δίνει τον πολλαπλασιαστή ολόκληρου αριθμού για τον εμπειρικό τύπο.
3. Πολλαπλασιάστε τους δείκτες στον εμπειρικό τύπο από τον πολλαπλασιαστή: Αυτό σας δίνει τη μοριακή φόρμουλα.
Συνοπτικά:
* Ο εμπειρικός τύπος σας λέει τον τύπο * και * τον σχετικό αριθμό των ατόμων σε μια ένωση.
* Ο μοριακός τύπος σας λέει τον * πραγματικό αριθμό * ατόμων σε ένα μόριο της ένωσης.
* Ο μοριακός τύπος είναι πάντα ένα πολλαπλάσιο του πλήρους αριθμού της εμπειρικής φόρμουλας.