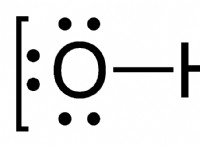Γιατί ένα άτομο οξυγόνου δεν μπορεί να σχηματίσει τριπλό δεσμό;
* ηλεκτρόνια σθένους: Το οξυγόνο διαθέτει έξι ηλεκτρόνια σθένους (ηλεκτρόνια στο εξωτερικό κέλυφος). Για να επιτευχθεί μια σταθερή ρύθμιση οκτάδων, πρέπει να κερδίσει δύο ακόμη ηλεκτρόνια.
* Χωρητικότητα συγκόλλησης: Κάθε ομοιοπολικός δεσμός περιλαμβάνει την κατανομή δύο ηλεκτρονίων. Το οξυγόνο μπορεί να σχηματίσει μέγιστο δύο ομοιοπολικούς δεσμούς, χρησιμοποιώντας τα δύο μη ζευγαρωμένα ηλεκτρόνια σθένους.
* Χωρίς κενά τροχιακά: Τα P-orbitals του Oxygen είναι γεμάτα με ηλεκτρόνια. Δεν υπάρχουν διαθέσιμα κενά τροχιακά για τη διαμόρφωση πρόσθετων ομολόγων.
* Απομάκρυνση: Οι τριπλοί δεσμοί περιλαμβάνουν σημαντική πυκνότητα ηλεκτρονίων στην περιοχή συγκόλλησης. Η απόρριψη μεταξύ των ηλεκτρονίων σε έναν τριπλό δεσμό θα ήταν πολύ υψηλή για το μικρό μέγεθος του οξυγόνου για να φιλοξενήσει.
Συνοπτικά: Η διαμόρφωση ηλεκτρονίων του οξυγόνου και η περιορισμένη χωρητικότητα συγκόλλησης εμποδίζουν την σχηματισμό τριπλών δεσμών.