Ποια είναι η κατάσταση οξείδωσης του χλωρίου;
Εδώ είναι γιατί:
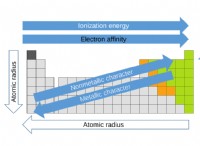
* Ηλεκτροργατιστικότητα: Το χλώριο είναι ένα εξαιρετικά ηλεκτροαρνητικό στοιχείο, που σημαίνει ότι έχει έντονη τάση να προσελκύει ηλεκτρόνια.
* Σχηματισμός ανιόντων: Όταν το χλώριο σχηματίζει ιοντικές ενώσεις με μέταλλα, κερδίζει ένα ηλεκτρόνιο για να επιτύχει μια σταθερή ρύθμιση οκτάδων, σχηματίζοντας το ιόν χλωριούχου (CL⁻). Σε αυτή την περίπτωση, η κατάσταση οξείδωσης είναι -1.
Ωστόσο, το χλώριο μπορεί επίσης να έχει άλλες καταστάσεις οξείδωσης, συμπεριλαμβανομένων:
* +1: Σε ενώσεις όπως το υποχλωριώδες οξύ (HOCL)
* +3: Σε ενώσεις όπως το χλωριώδες οξύ (HCLO₂)
* +5: Σε ενώσεις όπως το χλωρικό οξύ (HCLO₃)
* +7: Σε ενώσεις όπως το υπερχλωρικό οξύ (HCLO₄)
Η συγκεκριμένη κατάσταση οξείδωσης του χλωρίου σε μια ένωση εξαρτάται από τη φύση των άλλων ατόμων που συνδέεται με.