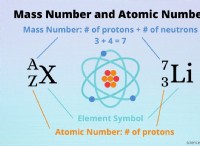
Η πιο συνηθισμένη κατάσταση οξείδωσης των στοιχείων στην ομάδα 2Α θα ήταν;
Εδώ είναι γιατί:
* Ηλεκτρονική διαμόρφωση: Τα στοιχεία της ομάδας 2Α διαθέτουν δύο ηλεκτρόνια σθένους (ηλεκτρόνια στο εξώτατο κέλυφος τους).
* Τάση να χάσετε ηλεκτρόνια: Έχουν μια έντονη τάση να χάσουν αυτά τα δύο ηλεκτρόνια σθένους για να επιτύχουν μια σταθερή, ευγενή διαμόρφωση αερίου.
* Σχηματισμός κατιόντων: Η απώλεια δύο ηλεκτρονίων έχει ως αποτέλεσμα το σχηματισμό ενός κατιόντων +2.
Παραδείγματα:
* beryllium (be): Να είναι
* μαγνήσιο (mg): Mg
* ασβέστιο (ca): Ca
* Strontium (SR): Sr
* βάριο (ba): Ba
* radium (ra): Ra
Ενώ ορισμένα βαρύτερα μέταλλα αλκαλικής γης μπορούν να παρουσιάσουν άλλες καταστάσεις οξείδωσης υπό συγκεκριμένες συνθήκες, το +2 είναι η πιο κοινή και σταθερή κατάσταση.