Τι δεν είναι ένας πραγματικός δεσμός, αλλά μάλλον μια έλξη μεταξύ μερικώς θετικού ατόμου υδρογόνου και αρνητικού ατόμου οξυγόνου ή αζώτου;
Εδώ γιατί δεν είναι ένας πραγματικός δεσμός:
* Οι πραγματικοί δεσμοί περιλαμβάνουν την κοινή χρήση ή τη μεταφορά ηλεκτρονίων: Οι ομοιοπολικοί δεσμοί περιλαμβάνουν την κατανομή των ηλεκτρονίων μεταξύ των ατόμων, ενώ οι ιοντικοί δεσμοί περιλαμβάνουν τη μεταφορά ηλεκτρονίων από το ένα άτομο στο άλλο.
* Οι δεσμοί υδρογόνου είναι ασθενέστεροι: Προκύπτουν από την ηλεκτροστατική έλξη μεταξύ ενός μερικώς θετικού ατόμου υδρογόνου και ενός μερικώς αρνητικού ατόμου (συνήθως οξυγόνου ή αζώτου) και είναι ασθενέστερα από τους αληθινούς ομοιοπολικούς ή ιοντικούς δεσμούς.
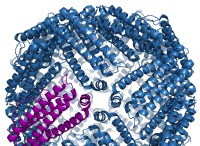
Έτσι, οι δεσμοί υδρογόνου δεν είναι αληθινοί δεσμοί, αλλά είναι σημαντικοί για πολλές βιολογικές διεργασίες. Βοηθούν στη συγκράτηση των κλώνων DNA μαζί, να σταθεροποιήσουν τη δομή της πρωτεΐνης και να επιτρέψουν στα μόρια του νερού να σχηματίσουν ισχυρές αλληλεπιδράσεις.