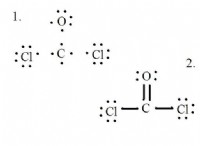Είναι διαλυτή το οξείδιο του νατρίου στο νερό;
Εδώ είναι γιατί:
* Ιονική ένωση: Το οξείδιο του νατρίου είναι μια ιοντική ένωση, που σημαίνει ότι σχηματίζεται από την ηλεκτροστατική έλξη μεταξύ θετικά φορτισμένων ιόντων νατρίου (Na+) και αρνητικά φορτισμένα ιόντα οξειδίου (o²⁻).
* πολικότητα του νερού: Το νερό (H₂O) είναι ένα πολικό μόριο, που σημαίνει ότι έχει ένα ελαφρώς θετικό άκρο (υδρογόνο) και ένα ελαφρώς αρνητικό άκρο (οξυγόνο). Αυτή η πολικότητα επιτρέπει στο νερό να αλληλεπιδρά έντονα με ιόντα.
* Διάλυση: Όταν το οξείδιο του νατρίου προστίθεται στο νερό, τα πολικά μόρια νερού περιβάλλουν τα ιόντα νατρίου και οξειδίου, σπάζοντας τους ιοντικούς δεσμούς που τους συγκρατούν στο στερεό. Τα ιόντα ενυδατωμένα (περιβάλλεται από μόρια νερού) και διασκορπίζονται σε όλο το διάλυμα.
αντίδραση με νερό:
Η διάλυση του οξειδίου του νατρίου στο νερό είναι μια εξωθερμική αντίδραση, που σημαίνει ότι απελευθερώνει θερμότητα. Σχηματίζει ένα διάλυμα υδροξειδίου του νατρίου (NaOH):
Na₂o (s) + h₂o (l) → 2 naOH (aq)
Σημαντική σημείωση: Η αντίδραση μεταξύ οξειδίου του νατρίου και νερού είναι αρκετά έντονη, παράγοντας πολλή θερμότητα. Είναι σημαντικό να χειριστείτε το οξείδιο του νατρίου με προσοχή.