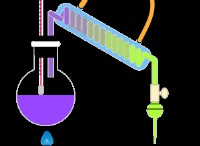
Τι μπορεί να ειπωθεί για ένα υγρό σημείου βρασμού;
Ορισμός:
* Ένα υγρό σημείου βρασμού είναι ένα υγρό στο σημείο βρασμού του, η θερμοκρασία στην οποία η πίεση του ατμού ισούται με την περιβάλλουσα ατμοσφαιρική πίεση.
Χαρακτηριστικά:
* Δυναμική ισορροπία: Στο σημείο βρασμού, ο ρυθμός των υγρών μορίων που διαφεύγουν στην αέρια φάση ισούται με τον ρυθμό των μορίων αερίου που επιστρέφουν στην υγρή φάση. Είναι μια κατάσταση ισορροπίας.
* σταθερή θερμοκρασία: Η θερμοκρασία ενός βρασμού υγρού παραμένει σταθερή, παρόλο που η θερμότητα προστίθεται συνεχώς. Αυτή η θερμική ενέργεια χρησιμοποιείται για να ξεπεραστεί οι διαμοριακές δυνάμεις που συγκρατούν τα υγρά μόρια μαζί.
* φυσαλίδες: Το βρασμό χαρακτηρίζεται από το σχηματισμό φυσαλίδων μέσα στο υγρό. Αυτές οι φυσαλίδες γεμίζουν με τον ατμό του υγρού και ανεβαίνουν στην επιφάνεια και διαφεύγουν.
* Εισαγωγή ενέργειας: Χρειάζεται πολλή ενέργεια για να βράσει ένα υγρό. Η ενέργεια που απαιτείται για τη μετατροπή ενός υγρού σε ένα αέριο ονομάζεται θερμότητα εξάτμισης.
* Πίεση ατμών: Η πίεση ατμών ενός υγρού είναι η πίεση που ασκείται από τον ατμό του όταν βρίσκεται σε ισορροπία με το υγρό. Στο σημείο βρασμού, η πίεση ατμών ισούται με τη γύρω ατμοσφαιρική πίεση.
Παράγοντες που επηρεάζουν το σημείο βρασμού:
* Διαμοριακές δυνάμεις: Τα υγρά με ισχυρότερες διαμοριακές δυνάμεις (όπως η δέσμευση υδρογόνου) έχουν υψηλότερα σημεία βρασμού.
* Πίεση: Το σημείο βρασμού μειώνεται καθώς η πίεση μειώνεται. Αυτός είναι ο λόγος για τον οποίο το νερό βράζει σε χαμηλότερη θερμοκρασία σε υψηλότερα υψόμετρα όπου η ατμοσφαιρική πίεση είναι χαμηλότερη.
* ακαθαρσίες: Η παρουσία ακαθαρσιών μπορεί μερικές φορές να επηρεάσει το σημείο βρασμού ενός υγρού, ειδικά εάν οι ακαθαρσίες διαλύονται στο υγρό.
Παραδείγματα:
* Το νερό βράζει στους 100 ° C (212 ° F) σε τυπική ατμοσφαιρική πίεση.
* Η αιθανόλη βράζει στους 78 ° C (173 ° F) σε τυπική ατμοσφαιρική πίεση.
Συνοπτικά: Ένα υγρό σημείου βρασμού είναι ένα υγρό στο σημείο βρασμού του όπου οι φάσεις υγρού και αερίου βρίσκονται σε ισορροπία, που χαρακτηρίζεται από σταθερή θερμοκρασία, σχηματισμό φυσαλίδων και σημαντική εισροή ενέργειας.