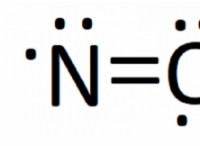Γιατί αναπτύσσεται ένα δίπολο σε μόριο;
1. Πολικοί ομοιοπολικοί δεσμοί:
* Ηλεκτροργατιστικότητα: Όταν δύο άτομα με διαφορετικές τιμές ηλεκτροαρνητικότητας σχηματίζουν έναν δεσμό, το περισσότερο ηλεκτροαρνητικό άτομο προσελκύει τα κοινά ηλεκτρόνια πιο έντονα. Αυτό δημιουργεί ένα μερικό αρνητικό φορτίο (δ-) στο πιο ηλεκτροαρνητικό άτομο και ένα μερικό θετικό φορτίο (Δ+) στο λιγότερο ηλεκτροαρνητικό άτομο.
* Παράδειγμα: Σε ένα μόριο νερού (H₂O), το οξυγόνο είναι πιο ηλεκτροαρνητικό από το υδρογόνο. Αυτό σημαίνει ότι το άτομο οξυγόνου τραβά τα κοινόχρηστα ηλεκτρόνια πιο κοντά στον εαυτό του, καθιστώντας το άκρο οξυγόνου του μορίου ελαφρώς αρνητικό και το υδρογόνο τελειώνει ελαφρώς θετικό.
2. Μοριακή γεωμετρία:
* Ασύμμετο σχήμα: Ακόμη και αν οι μεμονωμένοι δεσμοί μέσα σε ένα μόριο είναι μη πολικοί (ίση κοινή χρήση ηλεκτρονίων), το μόριο μπορεί ακόμα να έχει μια διπολική στιγμή εάν το μόριο έχει ασύμμετρο σχήμα. Αυτό οφείλεται στο γεγονός ότι οι μερικές χρεώσεις από τα μεμονωμένα ομόλογα δεν ακυρώνουν ο ένας τον άλλον.
* Παράδειγμα: Το διοξείδιο του άνθρακα (CO₂) έχει δύο πολικούς δεσμούς (C =O), αλλά το μόριο είναι γραμμικό. Οι διπολικές στιγμές των δύο ομολόγων ακυρώνουν ο ένας τον άλλον έξω, καθιστώντας το μόριο Nonpolar. Ωστόσο, το νερό έχει λυγισμένο σχήμα. Οι δύο πολικοί δεσμοί δεν ακυρώνουν ο ένας τον άλλον έξω, με αποτέλεσμα μια καθαρή διπολική στιγμή για ολόκληρο το μόριο νερού.
Συνοπτικά:
* πολικοί ομοιοπολικοί δεσμοί: Η διαφορά στην ηλεκτροαρνητικότητα μεταξύ των ατόμων δημιουργεί μερικές χρεώσεις.
* Ασύμμετο σχήμα: Μη ακύρωση μεμονωμένων διπόλων δεσμών λόγω της ανομοιόμορφης κατανομής της πυκνότητας ηλεκτρονίων.
Και οι δύο αυτοί παράγοντες συμβάλλουν στην ανάπτυξη μιας διπολικής στιγμής μέσα σε ένα μόριο. Αυτή η ροπή διπολικού μπορεί να έχει σημαντικές επιπτώσεις στις ιδιότητες του μορίου, συμπεριλαμβανομένης της διαλυτότητας, του σημείου βρασμού και της αλληλεπίδρασης με άλλα μόρια.