Ποια μάζα του HCl καταναλώνεται από την αντίδραση 2,50 moles μαγνήσιο στην εξίσωση Mg Plus ισούται με MgCl2 H2;
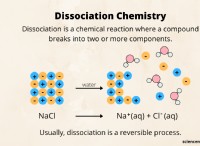
1. Ισορροπημένη χημική εξίσωση:
Η ισορροπημένη χημική εξίσωση για την αντίδραση είναι:
Mg + 2 HCl → Mgcl₂ + H₂
2. Αναλογία μολύβδου:
Η εξίσωση δείχνει ότι 1 mole mg αντιδρά με 2 moles της HCl.
3. Υπολογισμός:
* Έχετε 2,50 moles mg.
* Δεδομένου ότι η αναλογία mole είναι 1:2 (mg:HCl), χρειάζεστε διπλάσια ποσότητα HCl.
* Ως εκ τούτου, χρειάζεστε 2,50 moles mg * 2 moles hcl/1 mole mg =5,00 moles hcl.
4. Μάζα HCl:
* Η μοριακή μάζα του HCl είναι 1,01 g/mol (Η) + 35,45 g/mol (CL) =36,46 g/mol.
* Μάζα HCl =5,00 moles HCl * 36,46 g/mol HCl = 182,3 g HCl
Επομένως, 182,3 γραμμάρια HCl καταναλώνονται με την αντίδραση των 2,50 moles μαγνησίου.