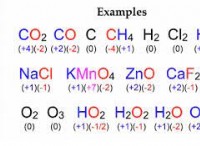
Ποιος είναι ο αριθμός οξείδωσης του N3H;
* Τυπικές καταστάσεις οξείδωσης του αζώτου: Το άζωτο έχει συνήθως καταστάσεις οξείδωσης που κυμαίνονται από -3 έως +5.
* Τυπική κατάσταση οξείδωσης του υδρογόνου: Το υδρογόνο συνήθως έχει κατάσταση οξείδωσης +1 (εκτός από μεταλλικά υδρίδια, όπου είναι -1).
Για να εξισορροπήσει τις φορτίσεις σε ένα μόριο, το άθροισμα των καταστάσεων οξείδωσης όλων των ατόμων πρέπει να ισούται με μηδέν. Είναι αδύνατο να επιτευχθεί αυτό με N3H.
Εδώ είναι γιατί:
* Αν υποθέσουμε ότι το άζωτο βρίσκεται στην πιο αρνητική του κατάσταση (-3), θα χρειαζόμασταν 3 άτομα υδρογόνου (+1 το καθένα) για να το εξισορροπήσουμε. Αυτό θα μας έδινε NH3 (αμμωνία), όχι N3H.
* Εάν το άζωτο βρίσκεται σε λιγότερο αρνητική κατάσταση, θα χρειαζόμασταν ακόμη περισσότερα άτομα υδρογόνου για να εξισορροπήσουμε το φορτίο, αποκλίνοντάς τον περαιτέρω από τον τύπο N3H.
Επομένως, το N3H δεν είναι σταθερή ένωση και δεν μπορούμε να αντιστοιχίσουμε αριθμούς οξείδωσης στα άτομα του.