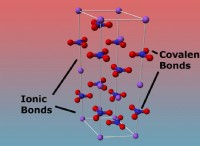
Πώς αντιδρούν τα οξέα;
Η αντίδραση:
Η αμμωνία (NH₃) είναι μια αδύναμη βάση, ενώ τα οξέα είναι δότες πρωτονίων (H⁺). Όταν ένα οξύ αντιδρά με αμμωνία, το οξύ δίνει ένα πρωτόνιο στο μόριο αμμωνίας, σχηματίζοντας ένα ιόν αμμωνίου (NH₄⁺). Το αρνητικά φορτισμένο ιόν από το οξύ συνδυάζεται στη συνέχεια με το ιόν αμμωνίου για να σχηματίσει ένα άλας.
Παράδειγμα:
* Υδροχλωρικό οξύ (HCl) + αμμωνία (NH₃) → Χλωριούχο αμμωνίου (NH₄Cl) + νερό (H₂O)
Επεξήγηση:
1. Μεταφορά πρωτονίων: Το ιόν υδρογόνου (Η) από HCl μεταφέρεται στο μόριο αμμωνίας (NH₃).
2. σχηματισμός ιόντων αμμωνίου: Το μόριο αμμωνίας δέχεται το πρωτόνιο και γίνεται ιόν αμμωνίου (NH₄⁺).
3. Σχηματισμός άλατος: Το ιόν χλωριδίου (CL⁻) από HCl συνδυάζεται με το ιόν αμμωνίου (NH₄⁺) για να σχηματίσει χλωριούχο αμμωνίου (NH₄Cl), ένα άλας.
Βασικά σημεία:
* εξουδετέρωση: Η αντίδραση μεταξύ ενός οξέος και μιας βάσης είναι μια αντίδραση εξουδετέρωσης, με αποτέλεσμα τον σχηματισμό αλατιού και νερού.
* Ιδιότητες άλατος: Τα άλατα αμμωνίου είναι συνήθως λευκά, κρυσταλλικά στερεά που είναι διαλυτά στο νερό.
* Εξοθερμική αντίδραση: Η αντίδραση μεταξύ οξέων και αμμωνίας είναι συνήθως εξωθερμική, απελευθερώνοντας θερμότητα.
Σημείωση: Η αντοχή του οξέος και η συγκέντρωση των αντιδραστηρίων μπορεί να επηρεάσουν τον ρυθμό και την έκταση της αντίδρασης.