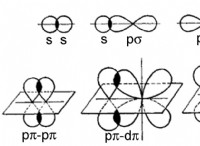
Τι είδους δεσμός είναι του 2;
* Ηλεκτροργατιστικότητα: Το φθόριο είναι το πιο ηλεκτροαρνητικό στοιχείο, ενώ το οξυγόνο είναι επίσης εξαιρετικά ηλεκτροαρνητικό. Αυτό σημαίνει ότι και τα δύο άτομα έχουν έντονη έλξη για τα ηλεκτρόνια.
* Κοινή χρήση, όχι μεταφορά: Αντί για ένα άτομο που παίρνει εντελώς ένα ηλεκτρόνιο από το άλλο (το οποίο θα σχηματίσει έναν ιοντικό δεσμό), μοιράζονται ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων.
* Polar Covalent: Ο δεσμός θεωρείται πολικός ομοιοπολικός Επειδή τα κοινόχρηστα ηλεκτρόνια τραβούν πιο έντονα προς τα άτομα φθορίου λόγω της υψηλότερης ηλεκτροαρνητικότητάς τους. Αυτό δημιουργεί ένα μερικό αρνητικό φορτίο στα άτομα φθορίου και ένα μερικό θετικό φορτίο στο άτομο οξυγόνου.