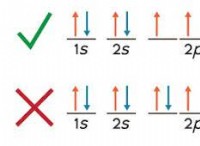
Ο πιο συνηθισμένος αριθμός συνδυασμένων οξυγόνου;
Εδώ είναι γιατί:
* Το οξυγόνο είναι εξαιρετικά ηλεκτροαρνητικό: Έχει έντονη τάση να κερδίζει ηλεκτρόνια.
* Σταθερή οκτάδα: Το οξυγόνο πρέπει να κερδίσει δύο ηλεκτρόνια για να επιτύχει ένα σταθερό οκτάτο (8 ηλεκτρόνια) στο εξωτερικό κέλυφος του.
* Εξαιρέσεις: Υπάρχουν μερικές εξαιρέσεις όπου το οξυγόνο έχει διαφορετικό αριθμό οξείδωσης:
* υπεροξείδια (όπως h₂o₂): Το οξυγόνο έχει αριθμό οξείδωσης -1.
* υπεροξείδια (όπως ko₂): Το οξυγόνο έχει αριθμό οξείδωσης -1/2.
* Οξυγόνο συνδεδεμένο με φθορίνη: Το οξυγόνο μπορεί να έχει έναν θετικό αριθμό οξείδωσης όταν συνδέεται με το εξαιρετικά ηλεκτροαρνητικό φθόριο (π.χ., στο Of₂, το οξυγόνο έχει αριθμό οξείδωσης +2).
Ωστόσο, στη συντριπτική πλειονότητα των ενώσεων, το οξυγόνο θα έχει αριθμό οξείδωσης -2.